M是生产某新型塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图,所示(图中球与球之间连线代表化学键单键或双键)。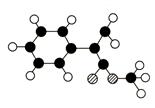
拟从芳香烃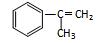 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
已知:M在酸性条件下水解生成有机物F和甲醇。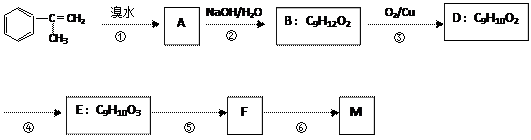
(1)根据分子结构模型写出M的结构简式
(2)写出②、⑤反应类型分别为 、
(3)D中含氧官能团的名称为 ,E的结构简式
(4)写出反应⑥的化学方程式(注明必要的条件) 。
(5分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)==2KCl+2MnCl2+5Cl2↑+8H2O
(1)在该反应中,氧化剂是_________ ,还原剂是_____________。(写名称)
(2)当有0.10mol电子发生转移时,被氧化的HCl的物质的量是 _____________。
有一种固体混合物,可能是由KNO3,K2SO4,KCl,CuCl2,CaCl2,和Na2CO3中的一种或几种组成,为了鉴别他们进行以下试验:
(1)将固体混合物溶于水,搅拌得无色透明溶液
(2)在此溶液中加入BaCl2溶液产生白色沉淀,过滤
(3)向上诉沉淀中加入足量的稀盐酸,沉淀全部消失。
(4)取(3)中滤液,滴加AgNO3有白色沉淀产生,且不溶于稀硝酸
推断:固体混合物中肯定含有
肯定没有
但不能判断出是否含有
阅读下列材料后,回答相应问题。
一个体重50Kg的健康人,含铁2g。这2g铁在人体中不是以单质金属的形式存在的,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利与铁的吸收。
(1)人体中经常进行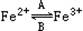 的转化,A中Fe2+做剂,B中Fe3+做剂。
的转化,A中Fe2+做剂,B中Fe3+做剂。
(2) “服用维生素C,可使食物中的三价铁离子还原成二价铁离子。”这句话指出维生素C在这一反应中做剂,具有性。
(6分)在下列物质
| A.:烧碱, | B.NH3.H2O, |
| C.SO3, | D.铁片,(E)食盐水,(F)甲烷, |
(G)醋酸,(H)碳酸钙中,
属于电解质的是____________,属于非电解质的是________________;
既不属于电解质又不属于非电解质___________ 。
根据图示回答下列问题:
(1)A、F 中所含官能团的名称分别是。
(2)反应②的条件是。反应②的反应类型为。
(3)反应③的化学方程式是。反应③的反应类型为。
(4)写出D的键线式 。
。
(5)F在铜催化下与氧气反应的化学方程式是。