铬是人体必需的微量元素,它与脂类代谢有密切联系,能增强人体内胆固醇的分解和排汇,但铬过量会引起污染,危害人类健康。不同价态的铬毒性不同,六价格的毒性最大,几乎是三倍铬毒性的100倍。下列叙述错误的是
| A.K2Cr2O7可以氧化乙醇,所以该反应常用于检查酒后驾驶 |
| B.污水中的铬一般为三价铬,但在溶解氧的作用下可被氧化为六价铬 |
| C.发生铬中毒时,可用维生素C缓解性,说明维生素C具有还原性 |
| D.配平Cr2O72-+I-+H+→Cr3++I2+H2O后,Cr3+的化学计量数是4 |
1mol某烃在氧气中充分燃烧,需要消耗氧气179.2 L(标准状况下)。它在光照的条件下与氯气反应能生成三种不同的一氯取代物。该烃的结构简式是
A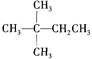 B CH3CH2CH2CH2CH3
B CH3CH2CH2CH2CH3
C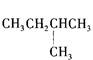 D CH3-
D CH3- -CH3
-CH3
丙烯醇(CH2=CH-CH2OH)可发生的化学反应有①加成②氧化③置换④加聚⑤取代
| A.只有①②③ | B.只有①②③④ |
| C.①②③④⑤ | D.只有①③④ |
将下列各种液体分别与溴水混合并振荡,不能发生化学反应,静置后混合液分成两层,溴水层几乎无色的是
A.氯水 |
B.己烯 |
| C.苯 | D.碘化钾溶液 |
下列物质中加入少量硝酸酸化的硝酸银溶液能得到沉淀的是
| A.溴乙烷 | B.氯水 |
| C.溴的CCl4溶液 | D.氯酸钾溶液 |
下列各物质中,最简式都相同,但既不是同系物,又不是同分异构体的是
| A.丙烯和环己烷 | B.乙烯和2﹣甲基丙烯 |
| C.丙炔和苯 | D.1﹣丁炔和1﹣丁烯 |