I2在KI溶液中存 在下列平衡:
在下列平衡:

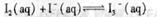
 某I2、KI混合溶液中,
某I2、KI混合溶液中,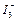 的物质的量浓度c(
的物质的量浓度c(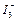 )与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是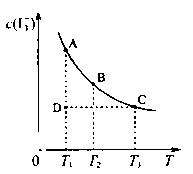


A.反应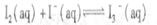 的△H>0 的△H>0 |
B.若温度T1、T2对应的平衡常数分别为K1、K2,则K1<K2 |
C.若反应进行到状态D时,一定有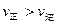  |
D.状态A与状态B相比,状态A的c(I2)大 |
X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是()

| A.该反应热化学方程式为X(g) +3Y(g) 2Z(g)△H=―(E2―E1) |
| B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线 |
| C.该温度下,反应的平衡常数数值约为533。若升高温度,该反应的平衡常数减小,Y的转化率降低 |
| D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线 |
X、Y、Z、W、E为原子序数相邻且依次递增的同一短周期元素(稀有气体除外),下列说法正确的是()
| A.若Y为非金属,则X一定为金属 |
| B.乙的氧化物常温下可能为液态 |
| C.X、E的简单离子的半径大小为X>E |
| D.若E的最高价氧化物对应的水化物的化学式为HmEOn,则其气态氢化物的化学式为H8-2n+mE或EH8-2n+m(m、n均为正整数) |
下述实验不能达到预期实验目的的是()
| 序号 |
实验内容 |
实验目的 |
| A |
向盛有10滴0.1mol/LAgNO3溶液的试管中滴加0.1mol/LNaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/LNa2S溶液 |
证明AgCl能转化为溶解度更小的Ag2S |
| B |
向2mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2 mL苯中加入3滴KMnO4酸性溶液,振荡 |
证明与苯环相连的甲基易被氧化 |
| C |
向Na2SiO3溶液中通入CO2 |
证明碳酸的酸性比硅酸强 |
| D |
向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 |
验证淀粉已水解 |
X、Y、Z、W有如右图所示的转化关系,且△H=△H1+△H2,则X、Y可能是()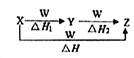
①C、CO②S、SO2
③AlCl3、Al(OH)3
④Na2CO3、NaHCO3⑤Fe、FeCl2
A.①②③④⑤ B.②④⑤
C.①③④ D.①②③
下列说法或表达正确的是()
①次氯酸的电子式为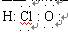
②含有离子键的化合物都是离子化合物
③强电解质溶液的导电能力一定比弱电解质溶液强
④丁达尔效应可用于区别溶液和胶体,运、雾均能产生丁达尔效应
⑤将金属a与外加直流电源的正极相连,将负极接到废铁上,可防止金属a被腐蚀
| A.①③⑤ | B.②④ | C.①②③ | D.④⑤ |