下表为长式周期表的一部分,其中的编号代表对应的元素。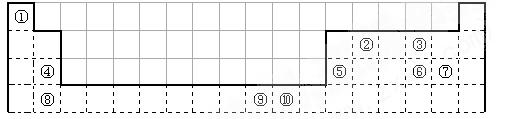
请回答下列问题:
(1)表中属于ds区的元素是 (填编号)。
(2)元素②与③形成的一种化合物是重要的化工原料,该化合物能使澄清石灰水变浑浊。有关该化合物分子的说法正确的是 。
| A.分子中含极性共价键 | B.属于非极性分子 |
| C.含有1个σ键和2个π键 | D.该化合物分子中,②原子采用sp2杂化 |
(3)根据上述表格 中的十种元素填空:
中的十种元素填空:
I、金属性最强的主族元素是_____________(填元素名称);
II、⑤、⑥、⑦的离子半径由小到大的顺序是_______________________(填化学式)
III、⑥、⑦两种元素的最高价氧化物对应的水化物的酸性由大到小的顺序是 _________
_________
(填化学式),
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为 _____________;该元素与元素①形成的分子X的空间构型为 。
家用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出表示丁烷燃烧的热化学方程式:
(8分) 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
请回答下列问题:(1)该反应的化学平衡常数K =。
(2)该反应为反应。(填“吸热”或“放热”)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为℃。
(4)830℃,在1 L的固定容器的密闭容器中放入2 mol CO2和1 mol H2,平衡后CO2的转化率为,
电解原理在化学工业上有广泛应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,
①电解池中X极上的电极反应式为_________________________________,
在X极附近观察到的现象为 。
②Y电极上的电极反应式 ,
检验该电极反应产物的方法是
。
(2)如果用电解方法精炼粗铜,电解液a选用CuSO4溶液(说明:杂质发生的电极反应不必写出)
①X电极的材料是________,电极反应式为___________________________ 。
②Y电极的材料是________,电极反应式为______________________________。
常温下有浓度均为0.05mol/L的四种溶液:①Na2CO3②NaHCO3
③HCl ④NH3·H2O,回答相关问题:
(1)上述溶液中,可发生水解的是(填序号)
(2)上述溶液中,既能与NaOH溶液反应,又能与H2SO4溶液反应的溶液中,离子浓度大小的关系
(3)向④中加入少量NH4Cl固体,此时c(NH4+/OH-)的值(“增大”、“减小”或“不变” )
(4)若将③和④的溶液混合后,溶液恰好呈中性,则混合前③的体积④的体积(“大于”、“小于”或“等于” )
(5)取10mL的③溶液,加水稀释到500mL,则此溶液中由水电离出的c(H+)=mol/
(1)实验室在配制氯化铁溶液时,常出现少许浑浊,原因离子方程式表示为 。为防止出现这样的现象,在配制时常加入
(2)根据下列2个热化学反应方程式:
FeO(s)+CO(g)=" Fe(s)+" CO2(g)△H= ―218kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g)△H= +640.5kJ/mol
写出CO气体还原Fe3O4固体得到Fe固体和CO2气体的热化学反应方程式:
______________
(4)常温下,等物质的量的浓度的①氨水②NH4HSO4③NH4Cl④(NH4)2CO3
⑤(NH4)2SO4溶液中,c(NH4+)由大到小的顺序为_____________________________(填序号)