如图是工业上采用离子交换膜法电解足量饱和食盐水的示意图。下列有关说法中不正确的是: 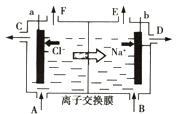
| A.从E口逸出的是氢气 |
| B.向B口中加入含少量NaOH 的溶液以增强导电性 |
| C.标准状况下每生成22.4LCl2,便产生2molNaOH |
| D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度 |
下列关于有机化合物的说法正确的是()
| A.乙醇和乙酸中都存在碳氧双键 | B.甲烷和乙烯都可以与氯气反应 |
| C.高锰酸钾可以氧化苯和甲烷 | D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
主链含5个碳原子,有甲基、乙基2个支链的烷烃有:()
| A.2种 | B.3种 | C.4种 | D.5种 |
已知:25℃,101KPa下,固体白磷、固体红磷分别充分燃烧,放出热量如下:
①P(s,白磷)+5/4 O2(g)=" 1/4" P4O10(s) 放出755.2kJ的热
②P(s,红磷)+5/4 O2(g)=" 1/4" P4O10(s) 放出738.5kJ的热
据此判断下列说法中正确的是
| A.由白磷变红磷是吸热反应 |
| B.白磷、红磷都是磷的单质,相互可以自由转化,不吸热,也不放热 |
| C.等质量时,白磷比红磷具有的能量高 |
| D.等物质的量时,断白磷分子中的键比断红磷分子中的键消耗的能量多 |
卤素间形成的化合物如“IF5、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应不正确的是
| A.IF5 + 3H2O = HIO3 +5HF |
| B.3IBr +2Fe = FeI3 + FeBr3 |
| C.BrCl的氧化性强于I2 |
| D.IBr可以与NaOH溶液反应生成2种盐 |
已知:断开1molN≡N需要吸收akJ热量,断开1molH—H需要吸收bkJ热量,断开1molN—H需要吸收ckJ热量。向某密闭容器中通入1molN2和3molH2,在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g)(放热反应)。下列描述中正确的是
2NH3(g)(放热反应)。下列描述中正确的是
| A.N2和H2具有的总能量一定比NH3具有的总能量低 |
| B.a、b、c三者的关系为:a+3b<2c |
| C.向密闭容器中通入1molN2和3molH2,反应放出的热量必为(6c―a―3b)kJ |
| D.形成1molN—H会放出ckJ热量 |