能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g)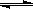 CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
(2)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的 倍。
(3)利用甲醇燃料电池设计如图所示的装置: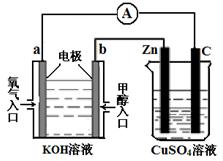
①则该装置中b为 极,写出装置中电解池内发生反应的离子方程式 ,
②当锌片的质量 变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
(4)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)="=" C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)="=" C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方程式 。
(7分)有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是_________。
(2)写出C元素基态原子的电子排布式_________________________。
(3)用轨道表示式表示D元素原子的价电子构型____________________。
(4)元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填“>”、“<”或“=”)
A、B、C、D四种短周期元素,0.5molA元素的离子得到的6.02×1023个电子后被还原为中性原子;0.4克A的氧化物恰好与100mL 0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等。A元素原子核外电子数比B元素原子核外电子数多1;C - 离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请填写下列空格:
(1)推断A、B、C、D四种元素的符号A_____;B____;C______;D_____。
(2)C的一价阴离子的结构示意图_____________________;
(3)D元素的最高价氧化物的结构式是:_______________;
(4)C、D两元素形成的化合物电子式 _____________,分子内含有_________键(填“极性”或“非极性”)。
(5)用电子式表示A、C两元素形成的化合物的过程:
______________________________________________________________。
(6)写出A的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的化学方程式:
用电子式表示下列过程:
①NaCl的形成过程____________________________________________
② H2O的形成过程____________________________________________
下列反应中,属于放热反应的是_____________,属于吸热反应的是___________。
| A.盐酸与烧碱溶液反应 | |
| B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑ | |
| C.氢气在氧气中燃烧生成水 | D.高温煅烧石灰石使其分解 |
E.铝和盐酸反应 F.葡萄糖在人体内氧化分解
(1)卤素元素包括______、______、______ 、______(填元素符号),随核电荷数递增,它们的原子半径依次_______,单质的氧化性依次_______。
(2)在1-18号元素中(稀有气体元素除外),元素所形成的最稳定的气态氢化物是________;与水或酸反应最剧烈的单质是________;最高价氧化物的水化物中碱性最强的碱是__________;最高价氧化物的水化物中酸性最强的酸是__________。(填化学式)