(10分)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
已知
①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是 ;若用同位素180示踪法确定反应产物水分子中氧原子的提供者,写出能表示180位置的化学方程式:
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 。
化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。图中所列装置是用燃烧法确定有机物分子式常用的装置。(每一组仪器只能使用一次)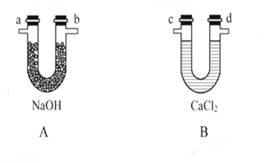

回答下列问题:
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是_____ 。
(2)C装置中浓硫酸的作用是_____ 。
(3)D装置中MnO2的作用是_____ 。
(4)若准确称取7.2 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加22 g,B管质量增加10.8 g,则该有机物的最简式为_____ 。
(5)要确定该有机物的分子式,则_____ (填“是”或“不”)需要测定其他数据,若能确定其分子式,若其一氯代物只有一种,则其结构简式为_____ 。
如图是某同学利用日常用品注射器设计简易实验装置。甲管中注入10 mL CH4,同温同压下乙管中注入 50 mL Cl2,将乙管气体推入甲管中,气体在甲管中反应,针管用日光照射一段时间。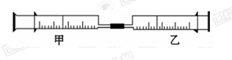
(1)下列是某同学预测的实验现象:
①气体最终变为无色;②实验过程中,甲管活塞向内移动;③甲管内壁有油珠;④产生火花。其中正确的是_____ 。
(2)甲管中发生的化学反应类型为_____ 。
(3)反应后,甲管中剩余气体能用下列试剂吸收的是___。
| A.水 | B.氢氧化钠溶液 |
| C.硝酸银溶液 | D.饱和食盐水 |
(4)反应后,若将甲管中的物质推入盛有适量AgNO3溶液的小试管中会观察到_____ ,若再向其中滴入几滴石蕊试液,又观察到_____ 。
用A、B、C三种装置都可制取溴苯,请仔细分析三套装置,并完成下列问题: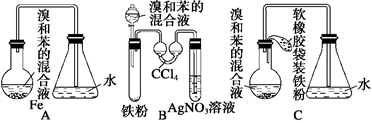
(1)写出三个装置中都发生的两个反应的化学方程式:
________________________________________________________________________,
________________________________________________________________________。
写出B的试管中还发生的反应的化学方程式:
________________________________________________________________________。
(2)装置A、C中长导管的作用是_______________________________________________。
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反应开始,对B应进行的操作是____________________________________________________,
对C应进行的操作是____________________________________________________。
(4)A中存在加装药品和及时密封的矛盾,因而在实验中易造成的不良后果是____________。
(5)B中采用了双球吸收管,其作用是____________________________________________;
反应后双球管中可能出现的现象是_________________________________________;
双球管内液体不能太多,原因是______________________________________________。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行,这两个缺点是________________________________________________________________________;
________________________________________________________________________。
已知浓硫酸与乙醇的混合液加热后可产生乙烯。为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:将生成的气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应。
乙同学在甲同学的实验中,发现褪色后的溶液中有硫酸根离子,推测在制得的乙烯中还可能有少量还原性气体杂质,由此他提出必须先除去,再与溴水反应。
请回答下列问题:
(1)甲同学实验中溴水褪色的主要的化学方程式为____________________________________
________________________________________________________________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生加成反应,理由是________。
a.使溴水褪色的反应未必是加成反应
b.使溴水褪色的反应就是加成反应
c.使溴水褪色的物质未必是乙烯
d.使溴水褪色的物质就是乙烯
(3)乙同学推测乙烯中必定含有的一种气体是________,可以用________来验证,这种气体与溴水反应的化学方程式是_____________________________________________。
(4)为验证溴水褪色的反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性的方法,理由是________________________________________________。
某化学课外小组用下图所示的装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。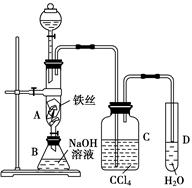
(1)写出A中反应的化学方程式:_____________________________________________。
(2)观察到A中的现象是___________________________________________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式: _____________________________________________________。
(4)C中盛放CCl4的作用是________________________________________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应。可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入________,现象是______________。