下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是
| A.在空气中敞口久置的浓硫酸,溶液质量增大(挥发性) |
| B.在加热条件下铜与浓硫酸反应(脱水性) |
| C.浓硫酸在白纸上书写的字迹变黑(氧化性) |
| D.浓硫酸可用来干燥某些气体(吸水性) |
右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,合这一情况的是 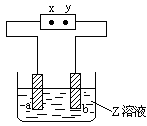
| a极板 |
b极板 |
x电极 |
Z溶液 |
|
| A |
锌 |
石墨 |
负极 |
CuSO4 |
| B |
石墨 |
石墨 |
负极 |
NaOH |
| C |
银 |
铁 |
正极 |
AgNO3 |
| D |
铜 |
石墨 |
负极 |
CuCl2 |
下列描述正确的是
| A.在pH=1溶液中,NH4+、K+、ClO—、Cl—可以大量共存 |
| B.MgO可以除去MgCl2溶液中的FeCl3 |
| C.足量铁粉与稀硝酸反应:Fe + 4H+ +NO3—== Fe3+ + 2H2O + NO ↑ |
D.对于平衡体系:H2(g)+I2(g)  2HI(g),其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深 2HI(g),其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深 |
下列有关电化学知识的描述正确的是
| A.CaO+H2O="=" Ca(OH)2可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa 固体 ⑤NaNO3溶液 ⑥KCl溶液
| A.②④⑤⑥ | B.①② | C.②③⑤ | D.②④⑥ |
现有等体积的Ba(OH)2、KOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,下列说法中正确的是( )
| A.若混合前三种溶液pH相等,将它们同等倍数稀释后,则KOH溶液pH最大 |
| B.若混合前三种溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3 |
| C.若混合前三种溶液物质的 量浓度相等,酸碱恰好完全中和时,则V1>V2>V3 |
| D.若混合前三种溶液pH相等,酸碱恰好完全中和时,则V1>V2>V3 |