在恒温下的密闭容器中,有可逆反应2NO(气)+O2(气) 2NO2(气),不能说明已达到平衡状态的是
2NO2(气),不能说明已达到平衡状态的是
| A.正反应生成NO2的速率和逆反应生成O2的速率相等 |
| B.反应器中压强不随时间变化而变化 |
| C.混合气体颜色深浅保持不变 |
| D.混合气体平均分子量保持不变 |
下图中X、Y分别是直流电源的两极,通电后发现a极极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是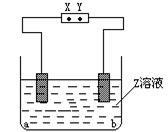
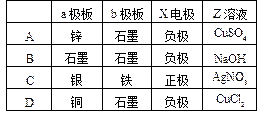
下列现象不能用胶体的知识解释的是
| A.牛油与NaOH溶液共煮,向反应后所得液体中加入食盐,会有固体析出 |
| B.一支钢笔使用两种不同牌号的蓝黑墨水,易出现堵塞 |
| C.向FeCl3溶液中加入Na2CO3溶液,会出现红褐色沉淀 |
| D.在河水与海水的交界处,有三角洲形成 |
在一密闭容器中进行反应:2SO2(气)+O2(气) 2SO3(固)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2 mol/L。当反应达平衡时,可能存在的数据是
2SO3(固)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2 mol/L。当反应达平衡时,可能存在的数据是
| A.SO2为0.4mol/L,O2为0.2mol/L |
| B.SO2为0.25 mol/L |
| C.SO2、SO3均为0.15 mol/L |
| D.SO3为0.4 mol/L |
在短周期中的X和Y两种元素可组成化合物XY3,则下列说法正确的是
| A.若X的原子序数是m,则Y的原子序数必定是m+4 |
| B.XY3晶体一定属于离子晶体 |
| C.X与Y可属于两个不同周期,也可属于同一周期 |
| D.X的原子半径小于Y的原子半径 |
重水(D2O)的离子积为1.6×10-15,可以用pH一样的定义来规定pD=-1g[D+],以下关于pD的叙述中,正确的是
| A.中性溶液中pD=7.0 |
| B.含0.01 mol的NaOD的D2O的溶液1L,其中pD= 12.0 |
| C.溶解0.01 molDCl的D2O的溶液1L,其pD=2.0 |
| D.在100ml 0.25 mol/ L的 DCl重水溶液中,加入 50ml0. 2 mol/L的NaOD的重水溶液,所得溶液的 pD=1.0 |