(15分)
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1="738kJ/mol " I2 =" 1451" kJ/mol I3 =" 7733kJ/mol " I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
⑴已知BA5 为离子化合物,写出其电子式 .
⑵B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形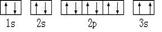 ⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
⑶某同学根据上述信息,推断C基态原子的核外电子排布为:
该同学所画的电子排布图违背了 .
⑷G位于 族 区,价电子排布式为 .
⑸DE3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型
为 .
⑹检验F元素的方法是 ,请用原子结构的知识解释产生此现象的原因是 .
⑺若某单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为 ,该单质晶体中原子的堆积方式为四种基本模式中的 .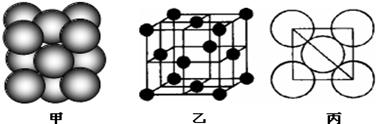
已知X为一种盐,A、C、D、F为无色气体,B常温常压下为无色无味的液体,I和Y为中学化学常见的单质,其中Y为气体,I为紫红色固体,E为黑色固体氧化物,L为蓝色沉淀。其中有些反应的条件及部分生成物被略去。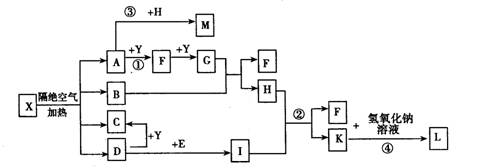
回答下列问题:
(1)写出C的电子式,L的化学式。
(2)写出反应①的化学反应方程式____;反应①一④中属于氧化还原反应的是。
(3)写出反应②的离子反应方程式____。
(4)M的水溶液呈酸性,其原因为(用离子方程式表示)____。
(5)利用电解可提纯I物质,在该电解反应中电解质溶液是____;写出阴极的电极反应式____。
(6)已知1 mol X在隔绝空气条件下分解产生的各产物的物质的量之比为A:B:C:D=2:1:1:1请推测A的化学式为____。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。
请回答下列问题:
(1)电池的负极材料为,发生的电极反应为;
(2)电池正极发生的电极反应为;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是,反应的化学方程式为;
(4)组装该电池必须在无水、无氧的条件下进行,原因是。
“西气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,两者的体积比约为1∶1。已知1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学反应方程式:_____________________,
若1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量_______890 kJ(填“>”、“=”或“<”)。
(2)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为_______;燃烧生成的CO2的质量比约为_______。
(3)以上数据和计算说明,以天然气代替水煤气作民用燃料,突出的优点是___________。
现有A、B、C、D、E五种物质,它们均含同一种元素,有以下转化关系:
已知A、B、C、X在常温下为气体,Z为液体,Y为紫红色金属,A与D的浓溶液相遇会产生白烟E。
请回答下面问题:
(1)写出A、Z的电子式AZ _____
(2)写出下列反应的方程式:
① A与D溶液反应的离子方程式
② A转化为B的化学方程式:
③已知A与C在一定条件下能反应,且生成两种没有污染的物质。请写出该反应的化学方程式。
A、B、C、D、E五种短周期主族元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素可形成两种固体,其中一种是淡黄色的固体X,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A元素在元素周期表中的位置,D的阴离子结构示意图,E的最高价氧化物对应的水化物是_______(填化学式)。
(2)B的氢化物沸点比D的氢化物沸点高,原因是。
(3)物质X的电子式,它与AB2反应的化学方程式。
(4)实验室制取E单质的离子方程式为____________________________。