已知X为一种盐,A、C、D、F为无色气体,B常温常压下为无色无味的液体,I和Y为中学化学常见的单质,其中Y为气体,I为紫红色固体,E为黑色固体氧化物,L为蓝色沉淀。其中有些反应的条件及部分生成物被略去。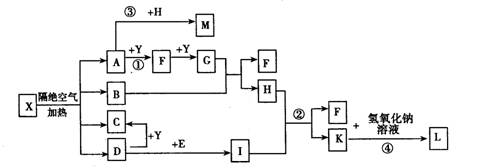
回答下列问题:
(1)写出C的电子式 ,L的化学式 。
(2)写出反应①的化学反应方程式_ ___;反应①一④中属于氧化还原反应的是 。
(3)写出反应②的离子反应方程式__ __。
(4)M的水溶液呈酸性,其原因为(用离子方程式表示)__ __。
(5)利用电解可提纯I物质,在该电解反应中电解质溶液是__ __;写出阴极的电极反应式___ _。
(6)已知1 mol X在隔绝空气条件下分解产生的各产物的物质的量之比为A:B:C:D=2:1:1:1请推测A的化学式为___ _。
请回答下列问题:
(1)下列现象和应用与电子跃迁无关的是________________________________。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱 E.石墨导电
(2)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍。某平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有_______个σ键。
(3)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有______(填元素符号),
②在a:苯 b:CH3OH c:HCHO d:CS2 e:CCl4 五种有机溶剂中,碳原子采取sp3杂化的分子有___________(填字母),CS2 分子的键角是__________。
分子的键角是__________。
③过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如 [Co(H2O)6]2+显粉红色。其中Co2+的价电子排布式为________________________
[Co(H2O)6]2+显粉红色。其中Co2+的价电子排布式为________________________
(4)利用CO可以合成化工原料COCl2,其中
①COCl2分子的结构式为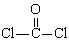 ,②COCl2分子内含有(填标号);
,②COCl2分子内含有(填标号);
A.4个σ键 B.2个σ键、2个π键
C.2个σ键、1个π键D.3个σ键、1个π键
下表为长式周期表的一部分,其中的编号代表对应的元素。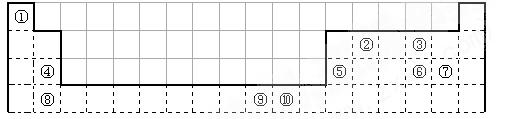
请回答下列问题:
(1)表中属于ds区的元素是(填编号)。
(2)元素②与③形成的一种化合物是重要的化工原料,该化合物能使澄清石灰水变浑浊。有关该化合物分子的说法正确的是。
| A.分子中含极性共价键 | B.属于非极性分子 |
| C.含有1个σ键和2个π键 | D.该化合物分子中,②原子采用sp2杂化 |
(3)根据上述表格 中的十种元素填空:
中的十种元素填空:
I、金属性最强的主族元素是_____________(填元素名称);
II、⑤、⑥、⑦的离子半径由小到大的顺序是_______________________(填化学式)
III、⑥、⑦两种元素的最高价氧化物对应的水化物的酸性由大到小的顺序是 _________
_________
(填化学式),
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_____________;该元素与元素①形成的分子X的空间构型为。
按要求填空
(1)在第二周期中(稀有气体除外),第一电离能最大的元素的原子结构示意 图是,第一电离能最小的元素的原子轨道表达式_______________________。
图是,第一电离能最小的元素的原子轨道表达式_______________________。
(2)第四周期元素中,4p轨道半充满的元素是_____________(填元素符号)
价电子层中s电子数与d电子数相同的元素是(填元素名称)。
(3)中国古代四大发明之一――黑火药,它的爆炸反应方程式为:
2KNO3+3C+S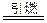 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除K、S外,上述方程式中出现的元素形成氢化物的稳定性从大到小依次为_____。
②写出K的基态电子排布式_____________________ _________________
_________________
抗击“非典”期间,过氧乙酸(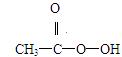 )是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
)是广为使用的消毒剂。它可由H2O2和冰醋酸反应制取,所以在过氧乙酸中常含有残留的H2O2。测定产品中过氧乙酸浓度c0。涉及下列反应:
① □MnO4-+□H2O2+□H+=□Mn2++□O2十□H2O
② H2O2+2 +2H+= I2+2H2O
+2H+= I2+2H2O
③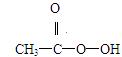 +2
+2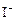 +2H+= CH3COOH+I2+H2O
+2H+= CH3COOH+I2+H2O
④ I2+2S2O32-= 2I-+S4O62-
请回答以下问题:
(l)配平反应①的离子方程式(配平系数填人以下方框内):
MnO4-+H2O2+H+="==" Mn2++O2十H2O
(2)用Na2S2O3标准溶液滴定I2时(反应④)选用的指示剂是________________________
(3)取b0 mL待测液,用硫酸使溶液酸化,再用浓度为a1 mol· 的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
的KMnO4标准溶液滴定其中的H2O2,耗用的KMnO4体积为b1 mL(反应①,滴定过程中KMnO4不与过氧乙酸反应)。
另取b0 mL待测液,加入过量的KI,并用硫酸使溶液酸化,此时过氧乙酸和残留的H2O2都能跟 KI反应生成 I2(反应②和③)。再用浓度为a2 mol· 的Na2S2O3标
的Na2S2O3标 准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
准溶液滴定生成的I2,耗用Na2S2O3溶液体积为b2 mL。
请根据上述实验数据计算过氧乙酸的浓度(用含a1、a2、b0、b1、b2的代数式表示)。
c0= ___________。
(4)为计算待测液中过氧乙酸的浓度c0,加入的KI的质量已过量但没有准确称量,是否影响测定结果 _______________(填是或否)
(13分)
 现有A、B、C、D、E、F六种化合物,已知它们的阳离子有
现有A、B、C、D、E、F六种化合物,已知它们的阳离子有 ,
, 阴离子有
阴离子有 ,现将它们分别配成
,现将它们分别配成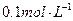 的溶液,进行如下实验:
的溶液,进行如下实验:
①
 测得溶液A、C、E呈碱性,且碱性为A>E>C;
测得溶液A、C、E呈碱性,且碱性为A>E>C;
②
 向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③
 向D溶液中滴加
向D溶液中滴加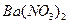 溶液,无明显现象;
溶液,无明显现象;
④
 向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
 根据上述实验现象,回答下列问题:
根据上述实验现象,回答下列问题:
(1)
 实验②中反应的化学方程式是
实验②中反应的化学方程式是
 (2)E溶液是,判断依据是
(2)E溶液是,判断依据是
 (3)写出下列四种化合物的化学式:A、C、
(3)写出下列四种化合物的化学式:A、C、
 D、F。
D、F。