一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
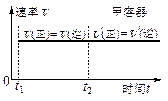
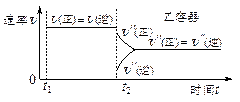
图1 图2 图3
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
有等体积、等pH值的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A.V3>V2>V1 C.B.V3=V2=V1 C.V3>V2=V1 C.D.V1=V2>V3
下列各组离子在指定环境中一定能大量共存的是
| A.使PH试纸显蓝色的溶液中:Cu2+、NO3-、Fe3+、SO42- |
| B.与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- |
| C.使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+ |
| D.PH=0的溶液中:Al3+、NH4+、Ca2+、ClO- |
已知反应:①101kPa时,2C(s)+O2(g)==2CO(g);ΔH="-221" kJ/mol
②稀溶液中,H+(aq)+OHˉ(aq)==H2O(l);ΔH="-57.3" kJ/mol,下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
已知 1mol白磷转化为红磷时放出 18.39 kJ的热量。在下列两个反应中:
4P(白、s)+ 5O2(g)=2P2O5(s);ΔH =" -" a kJ/mol(a > 0);
4P(红、s)+ 5O2(g)=2P2O5(s);ΔH =" -" b kJ/mol(b> 0)a 和 b 的关系为
| A.a < b | B.a = b | C.a > b | D.无法确定 |
用标准浓度的NaOH溶液来滴定未知浓度的盐酸,在下列操作中,会使盐酸测定浓度偏大的是
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③酸式滴定用蒸馏水洗净后,未用盐酸润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱试滴定管读数时,视线高于刻度线
| A.②③ | B.①③ | C.①④ | D.④⑤ |