下列说法不正确的是
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 |
| B. | 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 |
| C. | 氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量高 |
| D. | 放热反应有时也需要加热才可发生 |
反应X(g)+Y(g)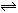 2Z(g)ΔH<0,达到平衡时,下列说法正确的是
2Z(g)ΔH<0,达到平衡时,下列说法正确的是
| A.减小容器体积,平衡向右移动 | B.加入催化剂,Z的产率增大 |
| C.增大c(X),X的转化率增大 | D.降低温度,Y的转化率增大 |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)  2HBr(g)
2HBr(g)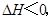 平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
| A.a>b | B.a=b | C.a<b | D.无法确定 |
下列说法不正确的是
| A.化学反应速率理论是研究怎样在一定时间内快出产品 |
| B.化学平衡理论是研究怎样使用有限原料多出产品 |
| C.化学反应速率理论是研究怎样提高原料转化率 |
| D.化学平衡理论是研究怎样使原料尽可能多地转化为产品 |
根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g) ΔH=-297.23kJ·mol-1,分析下列说法中不正确的是
| A.S的燃烧热为297.23kJ·mol-1 |
| B.S(g)+O2(g)=SO2(g)放出热量大于297.23kJ |
| C.S(g)+O2(g)=SO2(g)放出热量小于297.23kJ |
| D.形成1molSO2(g)的化学键释放的总能量大于断裂1molS(s)和1molO2(g)的化学键吸收的总能量 |
下列叙述中正确的是
| A.在稀溶液中,1mol酸和1mol碱完全反应所放出的热量,叫做中和热 |
| B.热化学方程式中,各物质前的化学计量数不表示分子个数 |
| C.在101kPa时,1mol物质燃烧时所放出的热量叫做该物质的燃烧热 |
| D.如果反应物所具有的总能量小于生成物所具有的总能量,则反应放热 |