利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知: §SO2(g)+1/2O2(g) SO3(g)+ 98 kJ
SO3(g)+ 98 kJ
(1)某温度下该反应的平衡常数K=10/3,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正)
v(逆)(填“<”、“>”或“=”)。
(2)一定温度下,向一带活塞的体积为20 L的密闭容器中充入0.4 mol SO2和0.2 mol O2,达到平衡后体积变为16 L,则平衡后SO2转化的百分率为 。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母)。
| A.保持温度和容器体积不变,充入0.2 mol O2 |
| B.保持温度和容器内压强不变,充入0.4 mol SO3 |
| C.降低温度 |
| D.移动活塞压缩气体 |
(4)若以下图所示装置,用电化学原理生产硫酸,为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为____________。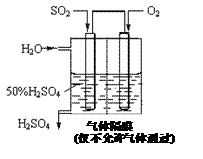
有如下两个反应: A 2HCl+Ba(OH)2===BaCl2+2H2O
B 2Fe3++Cu==2Fe2++Cu2+
(1)根据两反应的本质,判断能否设计成原电池:AB(填“能”或“不能”)不能设计成原电池的原因是
(2)根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池
①负极材料是,正极材料是,电解质溶液是
②写出负极的电极反应式
③若导线上转移电子0.2mol,则负极质量变化是
四种同类有机物A、B、C、D,它们的分子式均为C4H10O。已知A可被氧化为E,B可被氧化成F,C除可燃烧之外难以被氧化,A和C分别脱水后得到同一种不饱和烃,E和F都可发生银镜反应。
(1)D结构简式,F中所含官能团的结构式
(2)写出下列反应的化学方程式:(注明反应条件)
A → E:
C分子内脱水:
E发生银镜反应:
聚丙烯酸钠(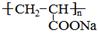 )是一种强吸水树脂。由某烃A合成聚丙烯酸钠的流程如下:
)是一种强吸水树脂。由某烃A合成聚丙烯酸钠的流程如下:
(1)A的名称为,B中官能团的名称是。
(2)物质E的结构简式是。
(3)反应②、③的反应类型分别为、。
(4)反应①发生的化学方程式为。
(5)写出符合下列条件的F的同分异构体(不考虑顺反异构)的结构简式。
a. 链状分子
b. 与新制氢氧化铜在加热条件下反应生成红色沉淀
c. 与NaOH溶液混合后滴入酚酞,加热,溶液颜色变浅
分子式为C8H13O2Cl的有机物A发生如图所示的变化: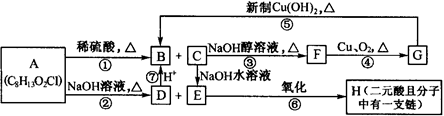
请回答下列问题:
(1)反应①和③的反应类型分别为:、
(2)请写出下列物质的结构简式: B; C
(3)请写出F与H等物质的量发生反应的化学方程式:
有机物A常用于食品行业。已知9.0 g A在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)A分子的质谱图如下图所示,从图中可知其相对分子质量是90,则A的分子式是______________________。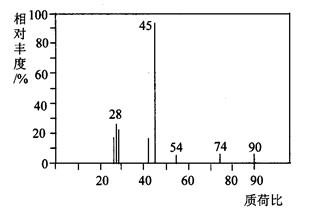
(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是__________________。
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是_________________________________。
(4)0.1 mol A与足量Na反应,在标准状况下产生H2的体积是__________L。
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是___________________________________________________________________。