已知2H2(g)+O2(g)===2H2O(l);ΔH=-569.6 kJ·mol-1,2H2O(g)===2H2(g)+O2(g);ΔH=+482.1kJ·mol-1。现有1 g液态H2O,蒸发时吸收的热量是
| A.2.43kJ | B.4.86kJ | C.43.8kJ | D.87.5 kJ |
下列事实不能用勒夏特列原理解释的是
| A.黄绿色的氯水光照后颜色变浅 |
| B.在硫酸亚铁溶液中,加入铁粉以防止氧化变质 |
| C.生产硝酸的过程中使用过量空气以提高氨气的利用率 |
| D.实验室常用排饱和食盐水的方法收集氯气 |
下列说法正确的是
| A.已知:2H2(g)+O2(g)=2H2O(l)△H<0,反应物总能量小于生成物总能量 |
| B.测定盐酸和氢氧化钠反应的中和热实验中,所用试剂可以是浓溶液 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ |
| D.已知C(s)与CO(g)的燃烧热分别为393.5kJ·mol-1 、283.0kJ·mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol |
下列有关化学反应速率的说法中,正确的是
| A.铁片与稀盐酸制取氢气时,加入NaNO3固体或Na2SO4固体都不影响生成氢气的速率 |
| B.等质量的锌片分别与同体积、同物质的量浓度的盐酸、硫酸反应,反应速率不相等 |
| C.SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D.加入反应物,单位体积内活化分子百分数增大,化学反应速率增大 |
下列有关能量转换的说法正确的是
| A.煤燃烧是热能转化为化学能的过程 |
| B.化石燃料和植物燃料燃烧时放出的热量均来源于太阳能 |
| C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 |
| D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
同温同压下,在4支相问体积的试管巾分別充有等体积的2种气体,它们是(1 ) NO和 O2 ( 2 ) NO2和 O2 ( 3 ) NO和 NO2 ( 4 )HCl和N2。现将4支试管均倒置于水槽中,充分反应后剩余气体的体积分别是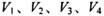 ,则下列关系正确的是
,则下列关系正确的是
A.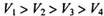 |
B.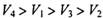 |
C.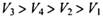 |
D.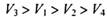 |