假设原子核外电子排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子 层电子的最大容量仍为2n2个。如果按此规律排布周期表,那么该周期表第3、4、5周期含有的元素分别有
层电子的最大容量仍为2n2个。如果按此规律排布周期表,那么该周期表第3、4、5周期含有的元素分别有
| A.5种,10种,15种 | B.8种,18种,18种 |
| C.8种,10种,15种 | D.9种,12种,15种 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd +2NiOOH +2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
有关该电池的说法正确的是
| A.放电时负极得电子,质量减轻 |
| B.放电时电解质溶液中的OH-向负极移动 |
| C.充电时阳极与外加电源的负极相连 |
| D.充电时阴极发生氧化反应 |
下列表示对应化学反应的离子方程式正确的是
| A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
B.用铜为电极电解饱和食盐水:2Cl—+2H2O Cl2↑+H2↑+2OH— Cl2↑+H2↑+2OH— |
| C.硫酸亚铁溶液被空气中氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
| D.小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH—=BaCO3↓+2H2O+CO32— |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol丙烷分子中,含有的非极性共价键数目为NA |
| B.标准状况下,1.8gH2O分子中所含有的电子数为NA |
| C.25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA |
| D.2.24L氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去)。
下列推断正确的是
A.若A是CaC2,X是H2O,则Y一定是溴水
B.若A是金属钠,X是H2O,则E一定能还原Fe2O3
C.若Y是NaOH,C是白色沉淀,则A与X一定发生置换反应
D.若Y是氧气,D是氧化物,则A与X一定发生氧化还原反应
下列有关实验装置的说法中正确的是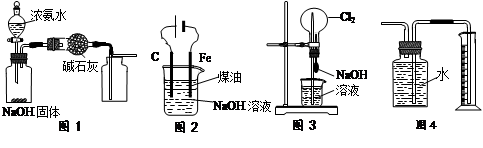
| A.用图1装置制取干燥纯净的NH3 |
| B.用图2装置实验室制备Fe(OH)2 |
| C.用图3装置可以完成“喷泉”实验 |
| D.用图4装置测量Cu与浓硝酸反应产生气体的体积 |