元素性质呈现周期性变化的根本原因是
| A.元素的相对原子质量递增,量变引起质变 |
| B.元素原子的核外电子排布呈周期性变化 |
C.元素 的原子半径呈周期性变化 的原子半径呈周期性变化 |
| D.元素的化合价呈周期性变化 |
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3③1s22s22p3④1s22s22p5。则下列有关比较中正确的是()
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>①>③=② |
下列说法错误的是( )
| A.1.5g CH3+中含有的电子数为0.8NA |
| B.Cu元素在元素周期表的ds区 |
| C.s轨道呈圆形,p轨道呈哑铃形 |
| D.DNA中的碱基互补配对是通过氢键来实现的 |
氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为( )
A.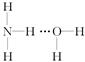 |
B.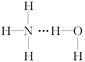 |
C.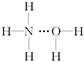 |
D.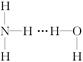 |
下列说法不正确的是( )
| A.能量高的电子在离核远的区域运动,能量低的电子在离核近的区域运动 |
| B.原子吸收光谱仪可用于测定物质中的金属元素,红外光谱仪可用于测定化合物的官能团 |
| C.分子间作用力比化学键弱得多,但它对物质的熔点、沸点有较大的影响,而对溶解度无影响 |
| D.同一元素的不同含氧酸,非羟基氧越多,该酸的酸性越强 |
实现下列变化时,需克服相同类型作用力的是()
| A.水晶和干冰的熔化 | B.食盐和冰醋酸的熔化 |
| C.液溴和液汞的汽化 | D.纯碱和烧碱的熔化 |