根据元素周期表和元素周期律,下列推断中错误的是
| A.砹是一种有色固体,它的气态氢化物很不稳定, |
| B.F2与水反应比Cl2与水反应剧烈 |
| C.铷的硫酸盐易溶解于水,其氢氧化物一定是强碱 |
| D.溴化氢比氯化氢稳定,HClO4酸性强于HBrO4 |
下列关于铜电极的叙述,正确的是()
| A.铜锌原电池中铜是负极 | B.用电解法精炼粗铜时粗铜作阴极 |
| C.在镀件上电镀铜时可用金属铜作阳极 | D.电解稀硫酸制H2、O2时铜作阳极 |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是()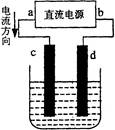
| A.a为负极、b为正极 | B.a为阳极、b为阴极 |
| C.电解过程中,d电极质量增加 | D.电解过程中,氯离子浓度不变 |
某反应2AB(g)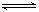 C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的ΔH、ΔS应为()
C(g)+3D(g)在高温时能自发进行,其逆反应在低温下能自发进行,则该反应的ΔH、ΔS应为()
| A.ΔH<0,ΔS>0 | B.ΔH <0,ΔS<0 | C.ΔH>0,ΔS>0 | D.ΔH>0,ΔS<0 |
1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为()
| A.C + H2O ="CO" + H2 ; ΔH=+131.3KJ·mol—1 |
| B.C(s)+ H2O(g) ="CO(g)" + H2(g) ; ΔH=+10.94KJ·mol—1 |
| C.C(s)+ H2O(l) ="CO(g)" + H2(g) ; ΔH=+131.3KJ·mol—1 |
| D.C(s)+ H2O(g) =CO(g) + H2(g) ; ΔH=+131.3KJ·mol—1 |
下列叙述中,正确的是
| A.能使溴水褪色的物质一定能和溴水发生加成反应 |
| B.天然蛋白质水解的最终产物是多种α—氨基酸 |
| C.能发生银镜反应的物质都是醛 |
| D.取淀粉和稀硫酸共热后的溶液中加入少量银氨溶液,水浴加热未发现银镜生成,证明淀粉尚未水解 |