按要求填空:
(1)写出表示含有8个质子,10个中子的原子的化学符号: 。
(2)在 1 1H、 2 1H、 3 1H中共有 种原子,它们能形成 种氢气分子。
(3)某简单微粒的结构示意图为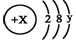 ,且X、Y 均为不大于20的正整数,据此回答下列问题:
,且X、Y 均为不大于20的正整数,据此回答下列问题:
①若呈电中性时该微粒不易与其它物质发生反应,这种微粒的符号是 ;
②若该微粒为一价阳离子,则x= ,该微粒表示的元素位于第 周期 族。
某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污染。流程如下:
回答下列问题:
(1)写出以石墨为电极电解饱和食盐水的离子方程式
(2)写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式,生成1mol四氯化钛时转移电子的物质的量为mol
(3)利用四氯化钛制备TiO2.xH2O时,需加入大量的水并加热的目的是
(4)钛广泛用于航天领域。氩气在冶炼钛的流程中的作用是
(5)利用CO和H2制备甲醇
①已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol。写出CO和H2制备甲醇的热化学方程式
②假设联合生产中各原料利用率为100%,若得到6mol甲醇,则只需再补充标准状况下的H2L
“百度百科:乙醇,俗称酒精,在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有酒香的气味,并略带刺激性,微甘。易燃,能与水以任意比互溶。用途很广,可用制造饮料、染料、燃料等。在国防工业、医疗卫生、有机合成、食品工业、工农业生产中都有广泛的用途。”根据所学知识回答下列问题
(1)书写乙醇催化氧化的产物和新制银氨溶液反应的化学方程式:
(2)在120℃,101kpa条件下,取ag乙醇在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量增加了bg,则ab(填“=”“>”“<”)
(3)乙醇燃料电池,KOH作电解质,书写负极电极反应式:
(4)请用所学知识解释为什么乙醇能和水以任意比互溶
亚磷酸(H3PO3)与足量的NaOH溶液反应生成Na2HPO3。
(1)亚磷酸是_______元酸。
(2)PCl3水解可制取亚磷酸:PCl3+3H2O=_________
(3)H3PO3溶液中存在电离平衡:H3PO3 H++H2PO3-
H++H2PO3-
①某温度下,0.10mol∙L-1的H3PO3溶液pH=1.6,即溶液中c(H+)=2.5×10-2mol∙L-1。求该温度下上述电离平衡的平衡常数K=_______。(只考虑H3PO3的第一步电离,结果保留两位有效数字。)
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH_____7(填“>”“=”“<”)
(4)亚磷酸具有还原性,可使碘水褪色。该反应的化学方程式为_______________。
(5)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下: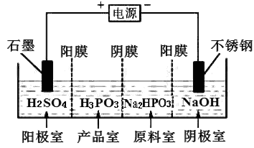
①阴极的电极反应式为__________。②产品室中反应的离子方程式为__________________。
肼(N2H4)是一种高能燃料,在工业生产中用途广泛。
(1)写出肼的电子式,1mol N2H4 中有个极性共价键。
(2)NH3与NaClO反应可以得到肼,该反应的化学方程式为。
(3)发射火箭时,肼(N2H4)为燃料,双氧水作氧化剂,两者反应生成氮气和气态水。
已知1.6g液态N2H4在上述反应中放出64.22kJ的热量,写出该反应的热化学方程式:_________。
(4)肼—空气燃料电池是一种碱性电池,该电池放电时负极反应式为。
(5)肼性质与氨气相似,易溶于水,可发生如下电离过程:
I、N2H4+H2O N2H5++OH— II、N2H5++H2O
N2H5++OH— II、N2H5++H2O N2H62++OH—
N2H62++OH—
①常温下,某浓度N2H6C12溶液的pH为5,则该溶液中由水电离产生的c(OH—)=。
②已知在相同条件下过程I的进行程度大于N2H5+ 的水解程度。常温下,若0.2 mol/L N2H4溶液与0.1 mol/L HCl溶液等体积混合,则溶液中N2H5+ 、N2H4·H2O、Cl—、OH—、H+粒子浓度由大到小的顺序为____________。
氯化铁是常见的水处理剂,无水FeCl3的熔点为555 K、沸点为588 K。工业上制备无水FeCl3的一种工艺如下: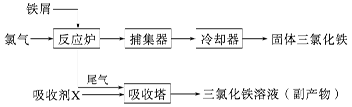
(1)取0.5 mL三氯化铁溶液滴入50 mL沸水中,再煮沸片刻得红褐色透明液体,该过程可用离子方程式表示为________________________________。
(2)已知六水合氯化铁在水中的溶解度如下:
| 温度/℃ |
0 |
10 |
20 |
30 |
50 |
80 |
100 |
| 溶解度 (g/100 g H2O) |
74.4 |
81.9 |
91.8 |
106.8 |
315.1 |
525.8 |
535.7 |
从FeCl3溶液中获得FeCl3·6H2O的方法是__________________________。
(3)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+ 开始沉淀;当溶液pH为4时,c(Fe3+)=__________mol·L-1 ( 已知:Ksp[Fe(OH)3]=1.1×10-36 ) 。
(4)吸收剂X是__________________;吸收塔中吸收剂X的作用是_______________________。
(5)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,再转移到100 mL容量瓶中,用蒸馏水定容; 取出10.00 mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用c mol·L-1 Na2S2O3溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去V mL。则样品中氯化铁的质量分数为____。