在室温条件下,向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述正确的是
| A.溶液中2c(Na+)=c(SO42-) | B.a/2 mol>沉淀的物质的量>0 |
| C.溶液中存在:c(Na+)+c(H+)=c(SO42-)+c(OH-) | D.原溶液中c(H2SO4) = a/2 mol/L |
下列实验能达到目的的是( )
| A.用CCl4萃取碘水中的碘 |
| B.将足量盐酸加入混有少量CaCO3杂质的Na2SO4中可除去杂质 |
| C.将混有少量HCl的Cl2通入NaOH溶液中除去HCl |
| D.将Fe(OH)3固体加入沸水中制备Fe(OH)3胶体 |
用下列实验装置进行相应实验,能达到实验目的的是( )
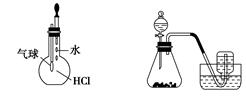
甲 乙 丙 丁
| A.装置甲:除去乙烯中混有的少量SO2 |
| B.装置乙:用浓硫酸配制1 mol/L的硫酸 |
| C.装置丙:检验HCl气体在水中的溶解性 |
| D.装置丁:用铜和浓硝酸反应制取NO2 |
下列实验所用的试纸不能预先用蒸馏水湿润的是( )
| A.用品红试纸检验SO2 |
| B.用淀粉碘化钾试纸检验Cl2 |
| C.用红色石蕊试纸检验氨气 |
| D.用pH试纸测定某溶液的pH |
下列各组中的两种有机物,无论以何种比例混合,只要混合物总质量不变,完全燃烧时生成水的质量就不变,符合这一条件的组合是( )
| A.CH3OH和C2H4O2 | B.C8H10和C4H10 |
| C.C2H4和C2H4O | D.C8H8和C4H8O3 |
酯类物质广泛存在于香蕉、梨等水果中。某实验小组先从梨中分离出一种酯,然后将分离出的酯水解,得到乙酸和另一种化学式为C6H14O的物质。对于此过程,以下分析中不正确的是( )
| A.C6H14O分子含有羟基 |
| B.C6H14O可与金属钠发生反应 |
| C.实验小组分离出的酯可表示为CH3COOC6H13 |
| D.不需要催化剂,这种酯在水中加热即可大量分解 |