现有三组混和物:①汽油和水;②碘和水;③硫酸钡和稀硫酸。分离以上各混和物的正确方法依次是: 、 、 。
. 有机化合物A的相对分子质量大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请回答:
⑴该化合物分子中含有个氧原子。
⑵化合物化学式为
⑶该化合物最多含有_______个羰基。
.根据下列信息写出符合要求的有机物的结构简式.
(1)若某有机物的分子量为128,若该有机物为链烃,则分子式为___________,若该烃一氯代物只有二种,则该烃的结构简式为______________或_____________,若该烃为芳香烃,则分子式为_____________,则该烃的结构简式为______________,若该有机物为烃的含氧衍生物,且是饱和一元的有机物,则其分子式为________________
(2)某有机物仅由C、H、O三种元素组成,且C、H、O原子个数之比为1:2:1,若该有机物为醛类,则其结构简式为:_______,若该有机物为羧酸,则其结构简式为_______,若该有机物为酯类,则其结构简式为_______,若该有机物为糖类,则其结构简式为_______,若该有机物分子式为C3H6O3,且两分子该有机物可形成六元环状酯,则C3H6O3结构简式为________________
. 核磁共振谱是测定有机物分子结构最有用的工具之一。瑞士科学家维特里希等三人即是利用核磁共振技术测定生物大分子的三维结构而获得2002年诺贝尔化学奖。在有机物分子中,不同位置的氢原子在核磁共振氢谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目。例如:乙醛的结构式为: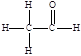 ,其PMR谱中有2个信号峰,其强度之比为3∶1。
,其PMR谱中有2个信号峰,其强度之比为3∶1。
⑴下列有机物分子中,在核磁共振氢谱中只给出一种峰(信号)的是()
| A.CH3-CH3 | B.CH3OCH3 | C.CH3CH2OH | D.CH3CH2Cl |
⑵化合物A和B的分子式都是C2H4Br2,A的PMR谱上只有1个峰,则A的结构简式为。
B的PMR谱上有个峰,强度比为
(3)化合物分子式是C8H10,含苯环,其多种同分异构体中有一种在PMR谱上只有3个信号峰,强度比为3:1:1,其结构简式为。
.提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| 括号内为杂质 |
除杂试剂 |
操作 |
|
| 1 |
乙炔(硫化氢) |
||
| 2 |
溴苯(溴) |
||
| 3 |
硬脂酸钠(甘油) |
||
| 4 |
乙醇(水) |
(10分) A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:H m D > H m C;② C m-、E (m-1)-具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1) HmDm的电子式_____________。
(2)还原性强弱:C m-___ E (m-1)-(填“>”或“<”);能证明其还原性强弱的离子方程式为:________。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:____________________。
(4) 常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式。在该溶液中溶质中含有的化学键类型是。
(5) 在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。