某温度时,在2L容器中X、Y、Z三种物质的物质的量(n)随着时间(t)变化的曲线如图所示。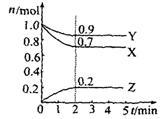
由图中数据分析:
(1)该反应的化学方程式为 。
(2)反应开始至2min,用Z表示的平均反应速率为 。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构 造如图所示:A、B两个电极均由多孔的碳块组成。
造如图所示:A、B两个电极均由多孔的碳块组成。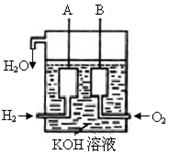
该电池的正极反应式为: ;
若该电池工作时增加了1mol H2O,电路中转移电子的物质的量为 。
(4)利用反应“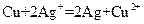 ”设计一个原电池(正极材料用碳棒)。回答下列问题:
”设计一个原电池(正极材料用碳棒)。回答下列问题:
①该电池的负极材料是________,发生________反应(填“氧化”或“还原”),负极的电极反应式为:____________,电解质溶液是________;
②正极上出现的现象是_____________________________;
③若导线上转移电子1  mol,则生成银________g。
mol,则生成银________g。
700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)  CO2(g)+H2(g);反应过程中测定的部分数据见下表(表中t2>t1),下列说法正确的是
CO2(g)+H2(g);反应过程中测定的部分数据见下表(表中t2>t1),下列说法正确的是
| 反应时间/min |
n(CO)/mol |
n(H2O)/mol |
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
0.20 |
A.反应在t1min内的平均速率为v(H2)=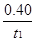 mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.40 mol
C.保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小
D.温度升高至800 ℃,上述反应平衡常数为0.64,则正反应为吸热反应
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为________________。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______________(写化学式),非金属气态氢化物还原性最强的是_________________(写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________(写出其中两种物质的化学式)。
(4) X2M的燃烧热ΔH =-a kJ·mol-1,写出X2M燃烧反应的热化学方程式:___________________________。
(5)ZX的电子式为___________;ZX与水反应放出气体的化学方程式为____。
(6)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为: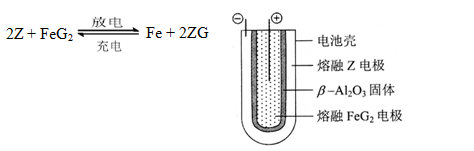
放电时,电池的正极反应式为_______________:
充电时,______________(写物质名称)电极接电源的负极;
该电池的电解质为___________________。
将CO2通入NaOH溶液中,所得产物随通入的CO2的物质的量的不同而不同。完成下列填空。
(1)250 mL 1 mol/L的NaOH溶液,最多可吸收CO2L(标准状况下)。
(2)向250 mL 2 mol/L的NaOH溶液中通入一定量CO2,溶液增重4.4 g,将所得溶液蒸干,计算所得固体中各成分的物质的量。
向未知浓度、体积为V L的 NaOH溶液中缓缓通入一定体积(标准状况下)的CO2,充分反应后,在减压低温的条件下蒸发溶液,得到白色固体。
(3)若反应中CO2和NaOH均无剩余,反应后向溶液中加入过量的澄清石灰水生成m1 g 白色沉淀。
①根据以上数据,用代数式表示CO2的体积V(CO2)=。
②根据以上数据,推理计算出NaOH溶液的浓度范围。
(4)写出确定NaOH浓度的实验步骤,并用代数式表示NaOH溶液的浓度。(设计实验方案时,只能用题中提供的CO2和NaOH溶液,不得使用其它化学试剂。)
实验步骤:。c(NaOH)=。
苯巴比妥是安眠药的成分,化学式为C12H12N2O3,分子结构中有两个六元环:下图是以A为原料合成苯巴比妥的流程示意图。完成下列填空。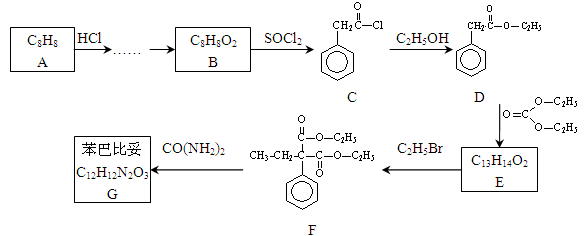
已知:①有机物D、E中亚甲基(—CH2—)的氢原子受羰基影响活性较高,容易发生如下反应: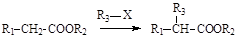
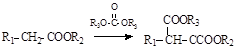
②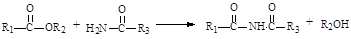
(1)芳香烃A与HCl反应后,制取B还需进行反应的类型依次为。
(2)一种酯与B互为同分异构体,且苯环上只有一个取代基,该酯同分异构体有种,写出其中一种结构系统命名。
(3)写出D 转化为E的化学方程式:
(4)苯巴比妥G的结构简式:
(5)E与CO(NH2)2在一定条件下合成的高分子结构简式:
(6)已知: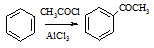 ,请设计合理方案以B的同系物
,请设计合理方案以B的同系物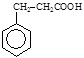 为原料合成
为原料合成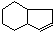 (用合成路线流程图表示为:A
(用合成路线流程图表示为:A B……
B…… 目标产物)。
目标产物)。
碳酸二甲酯(DMC)是一种低毒性的绿色化学品,可用于代替高毒性的光气(COCl2)作羰基化试剂。DMC的合成路线如下图。完成下列填空。
已知:RCOOR’ + R’’ OH → RCOOR’’ + R’OH
(1)写出反应类型:反应①反应③
(2)石油工业上获得C2H4的操作名称为。
(3)写出结构简式:DMC; X
(4)已知物质Y与DMC互为同分异构体,Y的水溶液呈酸性,在一定条件下2 molY能生成1mol分子中含六元环结构的有机物,则Y的结构简式为:
(5)DMC与双酚(  )在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式:。
)在一定条件下可生成芳香族聚碳酸酯,写出反应的化学方程式:。