(共20分)
Ⅰ:现有CH4、C2H4、C2H2、C2H6、C3H8五种有机物,回答下列问题:
⑴质量相同时:在相同状况下体积最大的是__ ___,完全燃烧时消耗O2的量最多的是__ _,
⑵同温同压同体积时,五种物质完全燃烧消耗O2的量最多的是__
Ⅱ:有机化学中的反应类型较多,将下列反应归类(填序号)。
①乙苯的制备:
②乙 烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色
烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色
⑤由乙烯制聚乙烯⑥甲烷与氯气在光照的条件下反应⑦溴乙烷和氢氧化钠溶液共热
⑧由甲苯制取TNT ⑨往苯酚钠溶液中通入CO2溶液中
(1)其中属于取代反应的是 ;属于氧化反应的是 ;
属加成反应的是 属于聚合反应的是
(2)写出⑦、⑧、⑨的化学方程式
⑦
⑧
⑨
在硬质玻璃管中的A、B、C处依次放有浸有KBr溶液、KI溶液、淀粉溶液的三个棉球(如图所示)由左端导入Cl2,在B处加热,可观察到A处棉球呈__________色,B处棉球呈______________色,C处棉球呈___________________色。
待试管冷却后,在B、C之间的玻璃壁上有__________色的___________,这是因为_______。
工业上从海水中提取溴可采用如下方法:
(1)向海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为__________。
(2)向上述混合液中吹入热空气,将生成的溴吹出用纯碱溶液吸收,其化学方程式为______________________________________________。
(3)将(2)所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后还可得到副产品Na2SO4。写出这一过程的化学方程式__________________。
(4)这样得到的溴中还混有少量Cl2,怎样除去(用离子方程式表示)____________。
在KI 淀粉溶液中,滴加少量Na2ClO溶液,并加入少量稀H2SO4,溶液立即变蓝,这是因为____________,离子方程式是________________。
在上述蓝色的溶液中滴加足量的Na2SO3溶液,蓝色逐渐消失,这是因为_________,离子方程式是________________________________________。
从以上实验可知,ClO-、I2、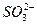 的氧化性由强到弱的顺序是_________________________。
的氧化性由强到弱的顺序是_________________________。
多原子分子氰(CN)2、硫氰(SCN)2和(OCN)2的性质与Cl2相似,它们也和Cl2一样可以生成酸和盐。见下表:
| 项目 |
氯气 |
氰 |
硫氰 |
① |
| “单质” |
Cl2 |
(CN)2 |
(SCN)2 |
(OCN)2 |
| 酸 |
HCl |
HCN |
② |
HOCN |
| 盐 |
KCl |
KCN |
KSCN |
③ |
(1)在表中①②③处应分别填写、、。
(2)完成下列化学方程式:
①HSCN+MnO2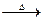
②(CN)2+H2O——
③(OCN)2+KOH——
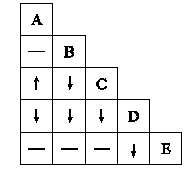
A、B、C、D和E五瓶溶液分别是HCl、CaCl2、Na2CO3、AgNO3、KI溶液中的一种,现将瓶内溶液各取少许进行两两混合实验,如果如下图所示,图中“↓”“↑”和“-”分别表示生成沉淀、气体和无明显变化,请根据实验现象判断各瓶内所装的溶液是A,B,C,D,E。