(1)现有浓度各为1 mol/L的FeCl3、FeCl2、CuCl2的混合溶液100mL,加入一定量的铁粉,按下列情况填空:
①充分反应后铁粉有剩余,则溶液中一定含有__________阳离子,一定没有__________阳离子。有关反应的离子方程式是__________________________
__________________________________________________________。
②充分反应后铁粉无剩余,有铜生成。则反应后的溶液中一定含有_________阳离子;溶液中可能含有_________阳离子,该阳离子在溶液中物质的量的可能存在范围是: ______________________。
③充分反应后,无固体沉淀物存在,反应后的溶液中一定含有____和____阳离子。
(2)现有AlCl3和FeCl3的混合溶液,其中Al3+和Fe3+的物质的量之和为0.1 mol。在此溶液中加入90 mL 4 mol / L的NaOH溶液,使其充分反应;设Al3+ 的物质的量与总物质的量的比值为x。
①根据反应的化学方程式计算x=0.4时,溶液中产生的沉淀是___________;物质的量是__________mol。
②计算沉淀中只有Fe(OH)3时的x的取值范围:_____________________。
在氢氟酸溶液中,存在如下电离平衡:HF H++F﹣
H++F﹣
(1)加入固体NaOH,电离平衡向 反应方向移动,c(H+) .
(2)加入固体NaF,电离平衡向 反应方向移动,c(H+) .
(3)升高温度,电离平衡向 反应方向移动,c(H+) .
食盐是日常生活的必需品,也是重要的化工原料。
粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO42―等杂质离子,实验室提供的试剂如下:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳。实验室提纯NaCl的流程如下: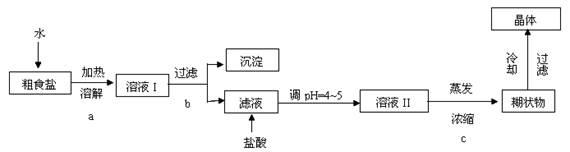
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42―离子,选出A所代表的多种试剂,按滴加顺序依次为i NaOH ii iii (填化学式)。
(2)请写出下列试剂加入时发生反应的离子反应方程式:
加入试剂i: ;
加入试剂iii: 。
(3)从NaCl溶液中得到NaCl晶体的操作步骤为 。
(4)实验中用到的盐酸的物质的量浓度为0.400mol/L,现实验室某浓盐酸试剂瓶上的有关数据如右:欲用上述浓盐酸配制实验所需浓度的稀盐酸480mL,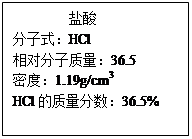
①配制需要的玻璃仪器有 (填仪器名称)
②需量取的浓盐酸的体积为: 。
已知反应:3NO2+H2O═2HNO3+NO,回答下列问题:
(1)该反应的离子方程式为 .
(2)氧化剂与还原剂的物质的量之比为 .
(3)在标准状况下,3.36L NO2与H2O完全反应转移的电子数目为 .
(4)用双线桥标出该反应中电子转移的方向和数目 .
交叉分类法就是将被分类的对象用 进行分类。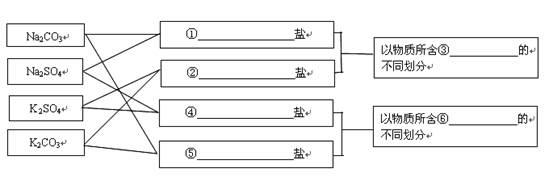
I.在反应:3Cu+□HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O中,请填写□中的数字是 。若有19.2 g铜被氧化,参加反应的HNO3的物质的量是___________mol,被还原的HNO3的物质的量是________mol,转移电子的数目为 。用单线桥标出该反应中电子转移的方向和数目:__________________
II.反应H2S+H2SO4(浓)=S↓+SO2↑+H2O中,氧化产物是 (填化学式)
反应6NO2+8NH3=7N2+12H2O中,氧化产物与还原产物的质量比是______________