锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的。因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂。某回收工艺流程如下: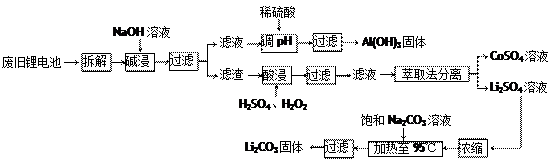
(1)上述工艺回收到的产物有Al (OH)3、 。
(2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是 。
(3)酸浸时反应的化学方程式为 。如果用盐酸代替H2SO4和H2O2的混合液也能达到溶解的目的,但不利之处是 。
(4)生成Li2CO3的化学反应方程式为 。已知Li2CO3在水中的溶解度随着温度的升高而减小,所以在浓缩结晶后要 过滤。
以下甲、乙、丙为探究原电池原理的有关装置,试回答下列问题: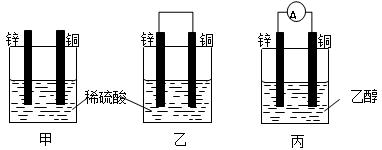
(1)甲中预计可以观察到得现象是:铜片上 (填“有”或“没有”)气泡产生,锌片上(填“有”或“没有”)气泡产生。
(2)乙中锌为原电池的极,电极反应是;铜为原电池的极,电极反应是。原电池总反应为
(3)丙中电流计A的指针是否发生偏转:(填“是”或“否”)
化学上常用一条短线来表示一对共用电子对,用元素符号和短线来表示物质结构的式子叫结构式,例如Cl2的结构式用Cl-Cl表示,H2O的结构式用H-O-H表示。
(1)写出下列物质的结构式:
①CO2②N2;③CH4;④C2H4。
(2)根据下列物质的结构式写出其相应的电子式:
①H―O―Cl_____;②H-O-O-H_______;
③ _____;④H-C≡C-H。
_____;④H-C≡C-H。
已知碳有两种常见的同位素126C、136C;氧有三种常见的同位素168O、178O、188O。
(1)由这五种微粒构成的CO的分子有种。
(2)本题中涉及种核素,种元素。
(3)一个相对分子质量最大的二氧化碳分子中有个电子,个中子;0.5 mol这种二氧化碳的质量是g。
金属钠是__________色金属,在空气中燃烧产物是__________,火焰呈__________色.将一块钠用小刀能切开,说明钠很__________,将切开的小块钠投入水中,发生反应的化学方程式为__________,现象是__________;在反应后的溶液中加入FeCl3溶液,反应的方程式为___________________________,反应的现象是_________________________.
现有A、B、C、D四种气体,A是密度最小的气体,B在通常情况下呈绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色 沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D。把无色无刺激气味气体C通入澄清石灰水时变浑浊。
(1)A、B、C、D的分子式分别为:A__________B_________C___________D_________。
(2)写出下列各反应的化学方程式:
A与B_______________________________________________
B与水_______________________________________________
B与NaOH溶液_______________________________________
C与澄清石灰水_______________________________________