短周期主族元素A、B、C、D的原子序数依次增大,A与D同主族,B与C在同一周期,B原子最外层电子数比C原子少2个, A、C单质在常温下均为气体,它们在一定条件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质在常温下能剧烈反应生成A的单质。所得溶液滴入酚酞显红色。回答下列问题:
⑴写出元素符号A ,B ,C ,D 。
⑵写出B与C两种单质完全反应后所得生成物的电子式 ,该分子空间构型为 。
⑶ C、D两种单质在点燃条件下形成的化合物的电子式 ,判断其中的化学键的类型 。
⑷写出两种由A、B、C、D四种元素组成的化合物的化学式 、 。
与甲醇燃料电池相比,乙醇燃料电池具有毒性低、理论能量密度高等优点,因此被广泛认为是更有前途的燃料电池。下图是一个乙醇燃料电池工作时的示意图。乙池中的两个电极均为石墨电极,乙池中盛有100 mL3.00 mol/L的CuSO4溶液。请回答下列问题: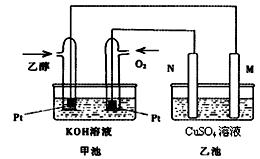
(1)在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出30kJ热量,表示该反应的热化学方程式为。
(2)N的电极反应式为。
(3)在此过程中,乙池中某一电极析出金属铜6.4g时,甲池中理论上消耗氧气升
(标准状况下)
(4) 在此过程中,若乙池中两电极产生的气体恰好相等时(假设标准状况 下),理论上需通入乙醇g?
下),理论上需通入乙醇g?
已知1 molCO气体完全燃烧生成CO2 气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)若1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量为890 kJ(填“>”、 “<”、“= ”)。
(2)若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的 取值范围是。
取值范围是。
(3)若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的取值范围是___________________________。
聚苯乙烯可用于制备高频绝缘材料,苯乙 烯在一定条件下存在如下图转化关系。
烯在一定条件下存在如下图转化关系。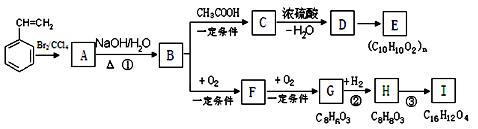
请回答下列问题:
(1)由苯乙烯合成这种高聚物的化学方程式为。
(2)反应①的反应类型是,C→D的反应类型是。
(3)C可能的结构简式有。
(4)H有多种同分异构体。同时符合下列条件的同分异构体共有种。
a. 与FeCl3溶液发生显色反应 b. 1 mol H最多能与3 mol NaOH反应;
c. 苯环上只有两个取代基。
(5)反应③的化学方程式是。
(10分)钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3•x H2O),写出铁发生电化学腐蚀时负极的电极反应:___________________________________。
(2)下列各个装置中铁棒被腐蚀由难到易的顺序是_______________(填字母)。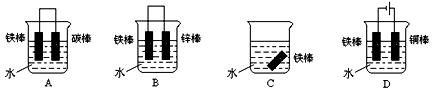
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图,请回答:
① A电极的电极反应式是 __
②若电镀前铁、铜两电极的质量相同,电镀完成后, 若电镀时
电路中通过的电子为0.2mol,将它们取出洗净、烘干、称量,则A、B两极质量相差____g。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
。
下列各化合物中,属于同系物的是(填入编号),属于同分异构体的是(填入编号)。
