(9分)下表为元素周期表的一部分,请回答有关问题:
| |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
|
|
|
|
① |
|
② |
|
| 3 |
|
③ |
④ |
⑤ |
|
⑥ |
⑦ |
⑧ |
| 4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)表中最活泼的金属是______,非金属性最强的元素是______;(填写元素符号)
(2) 最高价氧化物对应水化物酸性最强的化合物是__________;(填写分子化学式)
(3)表中能形成两性氢氧化物的元素是_______,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的离子反应方程式:
_____________________,___________________________;
(4)比较⑦、⑩单质氧化性的强弱:__________________________。
24.(12分)根据下列变化关系:
已知:E是一种具有果香味、难溶于水的物质,请填空:
(1)A物质的名称____________________。B溶液为__________________________.作用为__________________________________________
(2)写出④、⑥两步反应的化学方程式,在( )号中标明反应类型。
④ _______________________________________________________ ()
⑥_________________________________________________________ ()
23.(7分)对于CH4、C3H4、C2H4、C2H6、C3H6五种烃,回答下列有关问题:
(1)等质量的上述五种烃,在相同状况下体积最大的是______________。
(2)等质量的上述五种烃,完全燃烧生成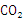 最多的是________________。
最多的是________________。
(3)在120 ℃、1.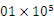 Pa条件下,与足量的
Pa条件下,与足量的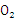 混合点燃,完全燃烧前后气体体积没有变化的烃是___________________________。
混合点燃,完全燃烧前后气体体积没有变化的烃是___________________________。
22、(9分)依据事实,写出下列反应的热化学方程式。
(1)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。 放出571.6kJ的热量,表示H2燃烧的热化学方程式为____________。
(2)在25℃、101kPa下,1g甲醇液体燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_______________________________________
(3)已知:已知:C(s)+O2(g)=CO2(g) ΔH="-437.3" kJ·mol一1
H2(g)+  O2(g)=H2O(g) ΔH="-285.8" kJ·mol一1
O2(g)=H2O(g) ΔH="-285.8" kJ·mol一1
CO(g)+  O2(g)=CO2(g) ΔH="-283.0" kJ·mol一1
O2(g)=CO2(g) ΔH="-283.0" kJ·mol一1
则煤的气化主要反应(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式是________________
21.有下列3种有机化合物A:CH2=CH2B: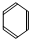 C:CH3COOH
C:CH3COOH
(1)写出化合物A、C中官能团的名称、______________;
(2)3种化合物中能使溴的四氯化碳溶液褪色的是(写名称);反应的化学方程为:;具有特殊气味、常做有机溶剂的是(写名称)。
(3)3种化合物中能与NaOH发生中和反应的是(写名称)。
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。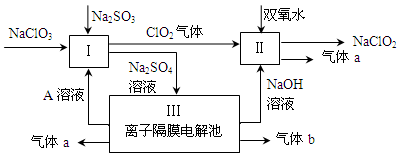
(1)Ⅰ、Ⅲ中发生反应的还原剂分别是、(填化学式)。
(2)Ⅱ中反应的离子方程式是。
(3)A的化学式是,装置Ⅲ中A在极区产生。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备。写出该制备反应的化学方程式。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量。(填“相同”,“不同”或“无法判断”)