将等物质的量A、B气体,置于容积为2L的密闭容器中发生反应,当反应进行到8s末,达到该反应的限度,测得A的物质的量减少0.6mol,B的物质的量减少0.2mol,C的物质的量增加0.4mol,此时n(A):n(B):n(C)=1:2:1。
则:
(1)该反应的化学方程式为: ;
(2)用生成物C表示的该反应的速率为: ;
(3)反应前A、B的物质的量浓度是: 。
下图涉及多种无机化工反应,所涉及物质都是由短周期元素组成,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F是人工合成的第一种有机物,且是一种常见的化肥材料,A、C、D、M均为常见元素的单质,“↑”表示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2:1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出洗净后加热分解可以得到B。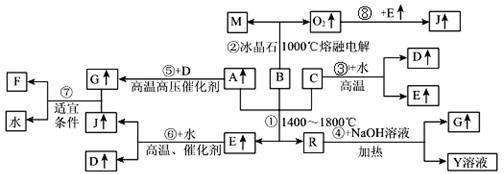
请回答下列问题:
(1)写出B化学式,F化学式:;G的空间构型。
(2)反应①的化学方程式为
(3)反应④的离子方程式为
(4)上述反应中属于非氧化还原反应的有(填写相应反应的序号)
(5)Y溶液呈性(填酸、碱或中),用离子方程式解释
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中溶质的pC=-lg1×10-3=3。下图为,H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:
(1)在人体血液中,HCO3-能起到稳定人体PH的作用,请用电解质溶液中的平衡解释:
(用方程式表示)。
(2)H2CO3一级电离平衡常数的数值Ka1
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1。c(CO32-)=0.075 mol·L-1,若t1时刻在上述体系中加入100 mL0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
(5)请画出t1时刻后Li+和CO32-浓度随时间变化关系图(用虚线表示Li+ ,实线表示CO32-)。
A为芳香烃衍生物,只含C、H、O三种元素,苯环上有两个处于邻位的取代基。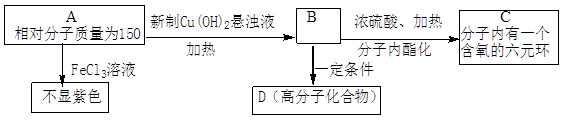
(1)B分子中含氧官能团的名称是。
(2)写出符合上述条件的A的两种可能的结构简式:;。
(3)等量的B分别与Na,NaOH,Na2CO3反应时,消耗三者物质的量之比是。
(4)符合上述条件的A,其中一种还可发生如下变化:
①A→ F的反应类型为。
②写出有关反应的化学方程式:
此A与新制Cu(OH)2悬浊液的反应:;
此A对应的B生成C的反应:。
1 molH2O中含有mol e—
0.1molNH4+中约含有个N,约含有个H.