做完“铁在氧气里燃烧”的实验后,小名同学有两个疑惑不解的问题,于是他进行了以下探究活动。
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)铁的氧化物均能溶于酸的溶液。
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入_____溶液,观察到的现象是_____,说明铁燃烧时溅落下来的黑色物质中还含有铁。
| |
Fe3O4 |
Fe2O3 |
铁 |
| 分解温度/℃ |
1538 |
1400 |
— |
| 熔点/℃ |
— |
— |
1535 |
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料2】
(1)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
(2)Fe2O3高温时分解成Fe3O4。
【理论探讨】
结合表中数据,可推知铁在氧气里燃烧时产生的高温应在_____之间,在此温度范围内_____已分解,所以铁在氧气里燃烧的产物是_____。
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须_____;
(2)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色_____,就说明包装盒破损进气,这样售货员就能及时发现并处理。
(3)下列铁的氧化物中,铁元素的质量分数由大到小的顺序是_____(填字母)。
A. FeO B. Fe2O3 C. Fe3O4
请分析、比较以下几组化学反应,得出结论。
| 组别 |
化学方程式 |
结论 |
| I |
|
反应物相同,生成物不同, 原因。 |
| II |
|
反应物相同,生成物不同, 原因。 |
| III |
|
反应物相同,生成物不同, 原因。 |
| IV |
(反应缓慢) (反应迅速) |
反应物相同,反应速率不同, 原因。 |
| 实践与应用 |
科学探究正努力实现对化学反应的控制,很多化学家致力于研究二氧化碳的"组合转化"技术,把过多二氧化碳转化为有益于人类的物质。若让二氧化碳和氢气在一定条件下反应,可生成一种重要的化工原料,反应的化学方程式如下: ,推断X的化学式是。 |
溶解度曲线为定量描述物质的溶解性提供了便利。下图是甲、乙两种物质的溶解度曲线。请据图回答:
(1)t1℃时甲物质的溶解度乙物质的溶解度(选填“>”、“=”、“<”);
(2)当甲物质的溶液中含有少量乙物质时,可以采用的提纯方法是;
(3)t2℃时,将甲、乙两种物质的饱和溶液各50克,分别蒸发掉10克水,甲溶液析出晶体的质量乙溶液析出晶体的质量(选填“>”、“=”、“<”)。
有"锂"走遍天下。锂电池广泛用于通信、电动车等行业,右图是锂的原子结构示意图和元素周期表中锂元素的部分信息,由此判断,锂原子在化学反应中易(选填"得到"或"失去")电子,写出锂离子的符号,氧化锂的化学式,氢氧化锂与盐酸反应是化学方程式。
如图是初中化学实验室常见气体的制取装置: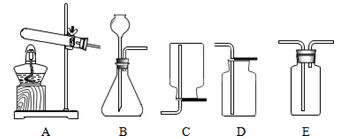
(1)实验室制取氧气的原理之一是(用化学方程式表示),此原理对应的发生装置是(填序号〕。用
装置收集氧气,验满的方法是;
(2)收集二氧化碳应选择的装置为(填序号)。理由是,欲收集一瓶干燥的二氧化碳,还需选用
装置,则
中应装入的药品是。
如图分别是水蒸气液化,水通电分解和氢气在氯气中燃烧的微观变化示意图.
请回答下列问题:
(1)图②表示的化学方程式为;
(2)从微观角度解释图①、图②的本质区别是;
(3)由图②、图③可得到:化学变化中一定不变的粒子是,可能发生改变的分子的。
(4)由图③还能获得的一条信息是。