下列物质的电子式书写正确的是
下列实验装置(固定装置略去)和操作正确的是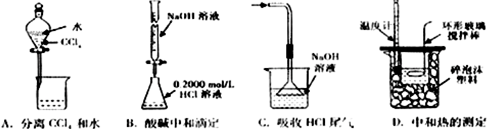
下列有关日常生活中涉及到的化学知识的描述不正确的是
| A.用煮面汤洗涤餐具上的油污 |
| B.用碘水检测土豆中含有淀粉 |
| C.用料酒清洗热水瓶中的水垢 |
| D.利用丁达尔效应区别鸡蛋清和食盐水 |
下列操作容易造成蔬菜中的维生素损失的是()
| A.洗菜:要先洗后切 |
| B.浸泡:切好的菜要浸泡半天,以除去残留农药 |
| C.切菜:要随切随炒,切忌切好后久置 |
| D.烹饪:烹调蔬菜时适当加点醋,可以减少维生素C的损失 |
在入住装修过的新房前,下列做法中错误的是()
A. 装修新房季节最好选择夏季
B.适度开窗通风,充分地进行内外空气对流
C.用高浓度的甲醛对室内环境消毒
D 在各个房间内均匀的放置适量的吊兰.芦荟等鲜花
2005年6月5日我国环境日主题是“人人参与,创建绿色家园”。下列说法不正
确的是()
| A.回收废旧电池 | B.加强控制燃放烟花爆竹法规 |
| C.停止使用含铅汽油 | D.将工厂烟囱加高,减少周围大气污染 |