原子序数11—17的元素,自钠到氯,电子层数相同,最外层电子数从 增加到 ,随着核电荷数依次递增,原子半径依次 ,核对外层电子的引力逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,因此,金属性逐渐 ,非金属性逐渐 。
G(异戊酸薄荷醇酯)是一种治疗心脏病的药物,其合成路线如下:
已知:
①A能与FeCl3溶液发生显色反应

(1)A的结构简式为____________。
(2)C烃基上的一氯代物有种(不考虑立体异构)____________。
(3)D分子中含有种不同化学环境的氢原子____________。
(4)写出同时符合下列条件的A的所有同分异构体的结构简式(不考虑立体异构):____________。
a.分子中有6个碳原子在一条直线上
b.分子中含一个—OH
(5)正戊醇可用作香料、橡胶促进剂等,写出以乙醇为原料制备CH3(CH2)3CHO的合成路线流程图(无机试剂任用)。合成路线流程示意图示例如下:
利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD。
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(—COOH)的反应。其中BAD结构简式为: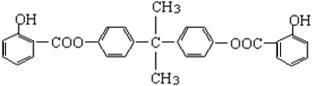
BAD的合成路线如下:
试回答下列问题:
(1)写出结构简式Y____________,D____________。
(2)属于加成反应的有____________(填数字序号)。
(3)1molBAD最多可与含____________molNaOH的溶液完全反应。
(4)写出方程式
反应④__________________。
F+E__________________。
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为____________种。
①能发生银镜反应 ②遇FeCl3溶液显紫色 ③核磁共振氢谱图中有四个吸收峰
据报导,目前我国结核病的发病率有抬头的趋势。抑制结核杆菌的药物除雷米封外,PAS—Na(对氨基水杨酸钠)也是其中一种。它与雷米封可同时服用,可以产生协同作用。已知:
① (苯胺,弱碱性、易氧化)
(苯胺,弱碱性、易氧化)
②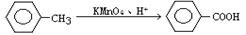
下面是PAS—Na的一种合成路线(部分反应的条件未注明):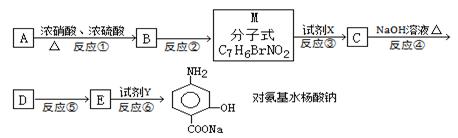
(1)A与浓硝酸和浓硫酸的混合物可以发生取代反应,在30℃时反应主要得到B和它的一种同分异构体,在一定条件下也可以反应生成TNT,请写出A制取TNT的化学方程式:__________________,TNT的系统命名法为__________________。
(2)写出反应②的化学方程式,注明反应条件并配平:__________________。
(3)本题中的中间产物M的官能团的名称为____________,与题中M具有相同官能团的同分异构体并属于芳香族化合物的共有____________种(不含M本身)(不考虑立体异构)。
(4)反应①的反应类型为__________________。
(5)试剂X为,试剂Y为__________________。
甘蔗渣可综合利用,回答下列问题。
Ⅰ.甘蔗渣可生成一种常见单糖A,A在乳酸菌的作用下生成有机物B,B经过缩聚反应生成可降解塑料,其结构简式为: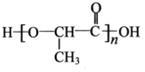
(1)A的分子式是____________;
(2)下列有关B的叙述正确的是____________(填序号);
A. B的分子式为C3H6O3
B. 1 mol B可与2 mol NaOH反应
C. 1 molB与足量的Na反应可生成1 molH2
(3)B在一定条件下可生成C,C能使溴的四氯化碳溶液褪色。B生成C的化学方程式是____________;
Ⅱ. 甘蔗渣还可生产一种重要的化工原料D,D的相对分子质量为90,1 mol D与足量NaHCO3反应放出标准状况下44.8 L CO2。
(4)D的官能团名称是____________;
(5)等物质的量的D与乙二醇在催化剂作用下可生成链状高分子化合物,其化学方程式是________________
苯甲酸和苯甲酸钠均是食品防腐剂。某化学学习小组的同学们尝试用甲苯的氧化反应制备苯甲酸,实验过程如下:按图示装置,在圆底烧瓶中放入适量甲苯和水,在石棉网上加热至沸,从仪器X上口加入适量高锰酸钾,继续煮沸并间歇摇动烧瓶,直到甲苯层消失,回流液不再出现油珠时停止反应。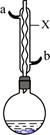
按如下流程分离出苯甲酸:
已知:① 苯甲酸熔点为122 ℃,沸点为249 ℃。
② 不同温度下苯甲酸在水中溶解度:4 ℃—0.18 g,18 ℃—0.27 g,75 ℃—2.2 g;
③
请回答下列问题:
(1)仪器X的名称是____________,冷却水应从口进入____________(填“a”或“b”)。
(2)分离苯甲酸的操作中,冰水浴冷却滤液的主要目的是____________,制得的苯甲酸晶体中可能含有的杂质是____________,为进一步提纯,应采用的方法是____________。
(3)芳香化合物A与苯甲酸分子式相同,A与NaOH溶液反应生成两种盐,该反应的化学方程式是____________。