 某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的Kw= 。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合。
某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的Kw= 。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合。
(1)若所得混合液为中性,且a=12,b=2,则Va︰Vb=  。
。
(2)若所得混合液为中性,且a+b=12,则Va︰Vb= 。
(3)若所得混合液的pH=10,且a=12,b=2,则Va︰Vb= 。
粉末状样品A是由等物质的量的MgO和Al2O3与常见金属氧化物B组成的混合物。A有如下图所示的转化关系。
请完成下列问题:
(1)单质C和H的化学式分别是__________、__________。
(2)写出由I生成J的离子方程式:_____________________________________
(3)写出由F生成G的离子方程式________________________________________
(4)若10.7 g样品A中MgO、Al2O3和B的物质的量均为0.05 mol,则B的化学式为_________。
某河道两旁有甲、乙两厂,它们排放的工业废水中,共含有K+、Ag+、Fe3+、 NO3- 、 Cl-、OH-六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是:
乙厂的废水中含有另外三种离子。如果加一定量(填“活性炭”、“硫酸亚铁”或“铁粉”),可以回收其中的金属是
2012年9月7日,云南省彝良地区连续发生5.7级地震,为了防止疫病流行,全国各地向灾区运送了大量的消毒剂、漂白剂等。过氧化物是很好的选择,下列有关过氧化物的相关问题:
(I)某一反应体系有反应物和生成物共五种物质: O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是。
(2)写出该反应的化学方程式,并标出电子转移的方向和数目
(3)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
(4分)现有
| A.二氧化硅 | B.三氧化二铁 | C.二氧化硫 | D.三氧化二铝。 |
请你根据已有的知识,选择合适的物质,用字母代号填空:
(1)能形成酸雨的是;(2)光纤制品的基本原料;
(3)属于两性氧化物的是;(4)红棕色固体是。
(11分下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D是海水中浓度最高的盐(部分反应物和生成物及水已略去)。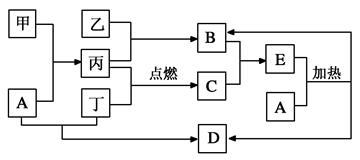
请回答下列问题:
(1)写出乙与丙生成B的化学方程式:________________________________________。
(2)写出甲和A溶液反应的离子方程式:_______________________________________。
(3)检验E中的阳离子时,取少量E于试管中,________________则证明E中有该阳离子。
(4)写出实验室制取B的化学方程式:______________________________________。
(5)B常用作工业制某酸的原料,写出由B制该酸过程中的化学方程式:
________________________________________________________。