某有机物甲和A互为同分异构体,经测定它们的相对分子质量小于100;将1mol甲在O2中充分燃烧得到等物质的量的CO2和H2O (g) ,同时消耗112LO2(标准状况);在酸性条件下将1 mol甲完全水解可以生成1 mol 乙和1mol丙;而且在一定条件下,丙可以被连续氧化成为乙。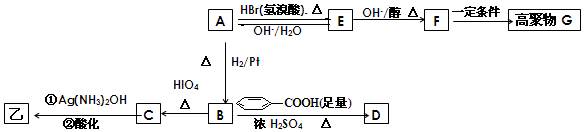
经红外光谱测定,在甲和A的结构中都存在C=O双键和C-O单键,B在HIO4存在并加热时只生成一种 产物C,下列为各相关反应的信息和转化关系:
产物C,下列为各相关反应的信息和转化关系: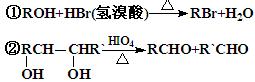
⑴ 请确定并写出甲的分子式 ▲ ;与甲属同类物质的同分异构体共有 ▲ 种(包含甲)。
⑵ E → F 的反应类型为 ▲ 反应;
⑶ A的结构简式为 ▲ ;G 的结构简式为 ▲ ;
⑷ B →D的反应化学方程式为 ▲ ;
⑸ 写出C在条件①下进行反应的化学方程式 ▲ 。
下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):
(1)写出乙的化学式、A的电子式、甲在周期表中位置是;
(2)写出G的一种用途;
(3)写出B与K反应的化学方程式:;
(4)整个转换过程中属于氧化还原反应的有个;
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式。
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量。回答下列问题:
H++MnO4-+H2C2O4→CO2↑+Mn2++□
(1)配平以上离子方程式,并在□中填上所需的微粒。
(2)该反应中的还原剂是。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为mol。 (4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(4)测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是。
②溶解沉淀时(能或不能)用稀盐酸,原因是。
③若消耗了1.0×10-4mol/L的KMnO4溶液20.00mL,则100mL该血液中含钙g。
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇。已知H2(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解5mol水消耗的能量是______kJ;
(2)写出甲醇燃烧热的热化学方程式:
(3)在容积为 2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况 下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于 300℃);
下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于 300℃);
下列说法正确的是(填序号)
①温度为T2时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=nB/tBmol·L- 1·min-1
1·min-1
②该反应在T1时的平衡常数比T2时的大
③该反应为吸热反应 ④该反应为熵增加的反应
④该反应为熵增加的反应
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中 ,充分反应达到平衡后,若容器内的压强与起始压强之比为0.8,则平衡时甲醇的体积分数为
,充分反应达到平衡后,若容器内的压强与起始压强之比为0.8,则平衡时甲醇的体积分数为
室温下取0.2 mol·L-1HCl溶液与0.2 mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)①混合溶液中水电离出的c(H+)__________0.2mol·L-1 HCl溶液中水电离出的c(H+);(填“>”、“<”、或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=__________ mol·L-1c(H+)-c(MOH) =__________ mol·L -1
-1
(2)室温下如果取0.2 mol·L-1 MOH溶液与0.1 mol·L-1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度________MCl的水解程度。(填“>”、“<”、或“=”),溶液中各离子浓度由大到小的顺序为_______________________。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。根据右图回答下列问题: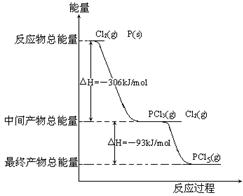
(1)P和Cl2反应生成PCl3的热化学方程式___________。
(2)PCl5分解成PCl3和Cl2的热化学方程式__________,
(3)P和Cl2分两步反应生成1molPCl5的△H3=______,P和Cl2一步反应生成1molPCl5的△H4_______△H3(填“大于”、“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是_____________________。