在恒温恒容容器中进行反应A(g)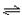 2B(g)
2B(g) +C(g),若A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
+C(g),若A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要的时间
| A.等于18 s | B.等于12  s s |
C.大于18 s | D.小于18 s |
下列推断正确的是()
| A.SiO2是酸性氧化物,能与NaOH溶液反应 |
| B.Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 |
| C.CO、NO、 NO2都是大气污染气体,在空气中都能稳定存在 |
| D.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
化学实验室进行的以下四个实验,下列有关说法中正确的是()
| 甲 |
100 mL 2.0 mol/L碳酸钠的溶液[ 200 mL 1.5 mol/L稀盐酸 |
盐酸逐滴加入到碳酸钠溶液中 |
| 乙 |
碳酸钠溶液逐滴加入盐酸到中 |
|
| 丙 |
50ml 1.0mol/L氯化铝溶液 75ml 2.5mol/L氢氧化钠溶液 |
氯化铝溶液逐滴加入到氢氧化钠溶液中 |
| 丁 |
氢氧化钠溶液逐滴加入到氯化铝溶液中 |
A.甲乙两组实验产生的气体量相同
B.丙丁两组实验产生的氢氧化铝沉淀量相同
C.甲乙两组实验现象相同
D.丙丁反应后的混合液中通入二氧化碳均无沉淀产生
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32—和Cl2反应的产物之一为SO42—。下列说法不正确的()
| A.该反应中还原剂是S2O32— |
| B.H2O参与该反应,且作氧化剂 |
| C.根据该反应可判断氧化性:Cl2 > SO42— |
| D.上述反应中,每生成l mol SO42—,可脱去2mol Cl2 |
CuCO3和Cu2(OH)2CO3的混合物34.6 g,可恰好完全溶解于300mL、2 mol·L-1的盐酸溶液中,若加热分解等量的这种混合物可得CuO固体质量为()
| A.16.0 g | B.19.2 g | C.24.0 g | D.30.6 g |
四支试管分别充满O2、NO2、C12、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满C12的试管是()
A B C D