(1)某化学小组的同学在学习了NaHCO3和Na2CO3的有关知识后,进行如下实验:在两支试管中分别加入3mL4 mol·L-1稀盐酸,将两个各装有0.3g NaHCO3或 Na2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3或Na2CO3同时倒入试管中,观察到现象如下: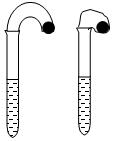
①试管中(填产生沉淀或气体及反应速率等相关现象)___________ _。
②盛______________的试管中气球变得更大,大小气球体积之比约为(填简单整数比)____________;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3
的试管温度有升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。类似如中和热,甲同学写出了下列热化学方程式:
HCO3-(aq)+H+(aq)=H2O(l)+CO2(g); △H>0
CO32-(aq)+2H+(aq)=H2O(l)+CO2(g); △H<0
甲下结论的方法是否正确____________(填“正确”或“不正确”)
(2)为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):
| 序号 |
试剂1 |
试剂2 |
混合前温度 |
混合后最高或最低温度 |
| ① |
35mL水 |
2.5g NaHCO3固体 |
20℃ |
18.5℃ |
| ② |
35mL水 |
3.2g Na2CO3固体 |
20℃ |
24.3℃ |
| ③ |
35mL 稀盐酸 |
含2.5g NaHCO3的饱和溶液32.5mL |
20℃ |
19℃ |
| ④ |
35mL 稀盐酸 |
含3.2g Na2CO3的饱和溶液23.1 mL+10ml水 |
20℃ |
24.2℃ |
| ⑤ |
35mL 稀盐酸 |
2.5gNaHCO3固体 |
20℃ |
16.2℃ |
| ⑥ |
35mL 稀盐酸 |
3.2g Na2CO3固体 |
20℃ |
25.1℃ |
请你帮助填写相关内容:
①该研究报告的题目是《_____________________________________》;
②该实验中所用的仪器除试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为_________和__________;通过上述实验可得出五条结论(用“吸热”或“放热”填写):
a:NaHCO3的溶解是_______过程;
b:Na2CO3的溶解是_______过程;
c:NaHCO3的饱和溶液和盐酸的反应是____________反应;
d:Na2CO3的饱和溶液和盐酸的反应是____________反应;
e:NaHCO3固体与稀盐酸反应的反应热是______(填a、b、c、d中的字母)的热效应之和。
某化学课外活动小组用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,正反应为放热反应,温度稍高即发生副反应6Cl2+
6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O。甲、乙、丙三人分别设计三个实验装置,如下图所示。
(1)请指出三个装置各处的缺点或错误(如没有可不填)
甲:_______________________________________________________;
乙:_______________________________________________________;
丙:_______________________________________________________。
(2)图甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号) ___________________________________。
(3)实验中若用12mol·L-1的浓盐酸100mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是小于0.15mol,其可能的主要原因是(假定各步反应均无反应物损耗且无副反应发生) _______________________________________________________。
拟用如图所示装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
| 气体 |
a |
b |
c |
d |
| C2H4 |
乙醇 |
浓H2SO4 |
NaOH溶液 |
浓H2SO4 |
| Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
| NH3 |
饱和NH4Cl溶液 |
消石灰 |
H2O |
固体NaOH |
| NO |
稀HNO3 |
铜屑 |
H2O |
P2O5 |
(1)上述方法中可以得到干燥、纯净的气体是____________________。
(2)指出不能用上述方法制取的气体,并说明理由。
①气体__________,理由是____________________。
②气体__________,理由是____________________。
③气体__________,理由是____________________。
( 12分 ) 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验: 先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。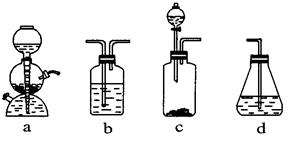
 b
b 
 b
b
(电石、水) ( ) ( ) ( 溴水 )
乙同学发现甲同学实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还有可能含有少量还原性的杂质气体。由此他提出必须先除去之,再与溴水反应。
请回答问题:
( 1 ) 写出甲同学实验中两个主要的化学方程式 _______________________________ 。
( 2 ) 甲同学设计的实验 ________ ( 填“能”或“不能” ) 验证乙炔与溴发生加成反应,其理由是 __________________________________________ 。
a. 使溴水褪色的反应,未必是加成反应
b. 使溴水褪色的反应,就是加成反应
c. 使溴水褪色的物质,未必是乙炔
d. 使溴水褪色的物质,就是乙炔
( 3 ) 乙同学推测此乙炔中必定含有的一种杂质气体是 ________ ,它与溴水反应的化学方程式是 __________________________ 。验证过程中必须全部除去。
( 4 ) 请你选用上列四个装置 ( 可重复使用 ) 来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。
( 5 ) 为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是什么?
( 12分 ) 已知两个羧基之间在浓硫酸作用下脱去一分子水生成酸酐,如:
某酯类化合物A是广泛使用的塑料增塑剂。A在酸性条件下能够生成B、C、D。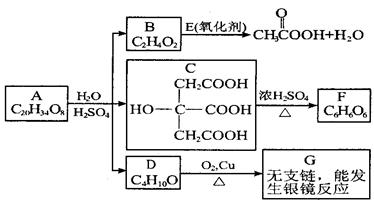
( 1 ) CH3COOOH称为过氧乙酸,写出它的一种用途 _________ 。
( 2 ) 写出 B + E  CH3COOOH + H2O 的化学方程式 ____________________ 。
CH3COOOH + H2O 的化学方程式 ____________________ 。
( 3 ) 写出F可能的结构简式 __________________ 。
( 4 ) 写出A的结构简式 ______________________ 。
( 5 ) 1 mol C分别和足量的金属Na、NaOH反应,消耗Na与NaOH物质的量之比是 _____ 。
( 6 ) 写出D跟氢溴酸 ( 用溴化钠和浓硫酸的混合物 ) 加热反应的化学方程式:
______________________________________________________ 。
( 8分 ) 有机物E和F可用作塑料增塑剂或涂料中的溶剂。它们的相对分子质量相等,可用以下方法合成: 
( 1 ) 请写出有机物的名称: A、_________ B _______________ 。
( 2 ) 请分别写出A + D E 和B + G
E 和B + G  F 的化学方程式: __________________ 。
F 的化学方程式: __________________ 。
( 3 ) X反应的类型是 _____________ ,X反应的条件是 _____________ 。
( 4 ) E与F的相互关系是 _______ ( 选填下列选项的编号 ) 。
①同系物 ②同分异构体 ③同一种物质 ④同一类物质