硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐。其化学式为:FeSO4•(NH4)2SO4•6H2O硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了。硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得。三种盐的溶解度(单位为g/100g水)如下表:
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
70 |
| (NH4)2SO4 |
73.0 |
75.4 |
78.0 |
81.0 |
84.5 |
91.9 |
| FeSO4•7H2O |
40.0 |
48.0 |
60.0 |
73.3 |
- |
- |
| 摩尔盐 |
18.1 |
21.2 |
24.5 |
27.9 |
31.3 |
38.5 |
如图是模拟工业制备硫酸亚铁铵晶体的实验装置

回答下列问题:
Ⅰ.(1)先用30%的氢氧化钠溶液煮沸废铁屑(含少量油污、铁锈、FeS等),再用清水洗净,用氢氧化钠溶液煮沸的目的是 。将处理好的铁屑放入锥形瓶中,加入稀硫酸,锥形瓶中发生反应的离子方程式可能为 (填序号)
A.Fe + 2H+=Fe2+ +H2↑ B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++H2S=2Fe2++S↓+2H+ D.2Fe3++Fe=3Fe2+
(3)利用容器②的反应,向容器①中通入氢气,应关闭活塞 ,打开活塞 (填字母)。容器③中NaOH溶液的作用是 ;向容器①中通人氢气的目的是 。
Ⅱ.待锥形瓶中的铁屑快反应完时,关闭活塞B、C,打开活塞A,继续产生的氢气会将锥形瓶中的硫酸亚铁(含极少部分未反应的稀硫酸)压到饱和硫酸铵溶液的底部。在常温下放置一段时间,试剂瓶底部将结晶出硫酸亚铁铵。硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,其原因是 ;从容器①中分离并得到纯净硫酸亚铁铵晶体的操作方法是 。
Ⅲ.制得的硫酸亚铁铵晶体中往往含有极少量的Fe3+,为测定晶体中Fe2+的含量,称取一份质量为20.0g的硫酸亚铁铵晶体样品,制成溶液。用0.5mo1/LKMnO4溶液滴定,当溶液中Fe2+全部被氧化,MnO‾4被还原成Mn2+时,耗KMnO4溶液体积20.00mL.滴定时,将KMnO4溶液装在 (填酸式或碱式)滴定管中,判断反应到达滴定终点的现象为 ;晶体中FeSO4的质量分数为 。
用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如图所示)
(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验中观察到C溶液中出现白色沉淀。则A中液体的是 (填名称),C中发生反应的离子方程式为 。
(2)若要制O2,B为黑色固体,A中的试剂是(填化学式),C中盛有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为血红色,写出C 中发生氧化还原反应的离子方程式 。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是 ,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为 。
实验室欲配制250mL 0.2 mol·L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取g碳酸钠晶体(Na2CO3•10H2O)。
(2)配制过程需要的仪器__________________ ______(填序号),还缺少的仪器有。
______(填序号),还缺少的仪器有。
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 |
| B.用托盘天平准确称取所需的Na2CO3•10H2O晶体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 |
| C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作______________;若定容时俯视刻度线_______________。
1,2-二溴乙烷可做抗爆剂的添加剂,常温下为无色液体,密度为2.18g cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题:
cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题: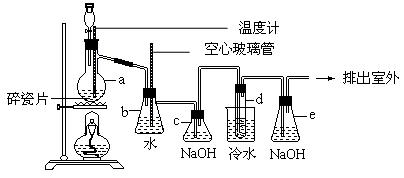
(1)写出制备1,2—二溴乙烷的两个反应方程式:
______________________________________、。
(2)安全瓶b可以防止倒吸,并用于检查实验进行时试管d是否发生堵塞,请写出发生堵塞时b的现象:_________________________________________。
(3)容器c中NaOH溶液的作用是: __________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出很多。如果装置的气密性没有问题,试分析其可能的原因。
(5)e装置内NaOH溶液的作用是:__________________________________。
味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠(化学式为C5H8NO4Na)。谷氨酸钠有鲜味,易溶于水。某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl含量≤20%”。某学校化学科研小组现对此味精中NaCl的含量进行测定。
Ⅰ.查阅资料:谷氨酸钠的存在不影响NaCl含量的测定。
Ⅱ.设计实验方案:
(1)实验试剂:水、试剂X的溶液等
(2)实验过程: [
[
根据上述实验步骤回答下列有关问题:
①试剂X是,其作用是。
②操作(1)所需要的玻璃仪器有。
③操作(2)的名称 是。
是。
④通过计算判断该味精中NaCl的质量分数,是否符合其包装上标注的标准。
⑤如果溶液A为50 mL,则溶液A中NaCl的物质的量浓度是多少?
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
(1)写出下列仪器的名称:
①_____________②______________③______________④______________
(2)仪器①~④中,使用时必须检查是否漏水的有________(填序号)具体检查方法是_________________________________________________________________________________。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有____________,将仪器补充完整后进行的实验操作的名称为:_______________;使用时进水口为______(填f或g)。现需配制800mL 0.2 mol/L NaOH溶液,某该同学用托盘天平称取6.4克NaOH固体,其中装置II是该同学转移溶液的示意图,该同学操作的错误是
_