已知[Co(NH3)6]3+呈正八面体结构,若其中有两个NH3分子分别被Cl-和H2O取代,所形成的[Co(NH3)2Cl2(H2O)2]3+的几何异构体种数有(不考虑光学异构)几种( )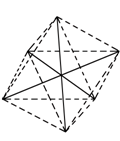
| A.3种 | B.4种 | C.5种 | D.6种 |
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g),甲醇生成量与时间的关系如下图所示。
CH3OH(g),甲醇生成量与时间的关系如下图所示。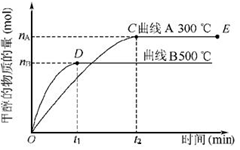
下列有关说法正确的是( )
| A.在300 ℃条件下,t1时刻该反应达到化学平衡 |
| B.在500 ℃条件下,从反应开始到平衡,氢气的平均反应速率v(H2)为nB/(3t1) mol/L |
| C.在其他条件不变的情况下,将处于E点的体系体积压缩到原来的1/2,则氢气的浓度减小 |
| D.由图像说明该反应的正反应为放热反应 |
一定温度下,在固定体积的密闭容器中发生可逆反应 A(s)+2B(g) 2C(g) ,下列叙述中是反应达到平衡的标志的是( )
2C(g) ,下列叙述中是反应达到平衡的标志的是( )
(1)v正(A)=2v逆(C);(2)单位时间生成amol A,同时生成2amol B;(3)A、B、C的浓度不再变化;(4)混合气体的平均摩尔质量不再变化(5)混合气体的总压强不再变化;(6)A、B、C的分子数目比为1:3:2。
A.(1)(3)(4)B.(3)(4) C.(2)(3)(5) D.(3)(4)(5)(6)
某酸甲溶液的pH=2,某酸乙溶液的pH=3,下列说法正确的是( )
| A.若甲为强酸、乙为弱酸,则c(甲) :c(乙)="10" :1 |
| B.若甲为弱酸,乙为强酸,则一定满足c(甲)>c(乙) |
| C.若甲为强酸,乙为弱酸,则其物质的量浓度不可能相等 |
| D.若甲、乙均为弱酸,则甲酸的电离常数一定比乙酸大 |
浓度均为0.1mol/L的三种溶液:①氨水②盐酸③氯化铵溶液,下列说法不正确( )
| A.PH由大到小的顺序:② > ③ > ① |
| B.水电离的C(H+):③ > ① > ② |
| C.C(NH4+):③ > ① |
| D.①②等体积混合后的溶液:C(H+)>C(OH-) |
化学反应可视为旧化学键断裂和新化学键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是a kJ?mol-1,H—H键的键能是b kJ?mol-1;由N2和H2合成1 mol NH3时可放出c kJ的热量。那么N—H 键的键能是( )
| A.(a+3b-2c)/2 kJ?mol-1 | B.(a+3b+2c)/6 kJ?mol-1 |
| C.(a+3b-2c)/6 kJ?mol-1 | D.(a+3b+2c)/3 kJ?mol-1 |