元素性质呈周期性变化的决定因素是 ( )
| A.元素原子半径大小呈周期性变化 | B.元素相对原 子质量依次递增 子质量依次递增 |
| C.元素原子核外电子排布呈周期性变化 | D.元素的最高正化合价呈周期性变化 |
甲苯(C7H8)和甘油(C3H8O3)组成的混合物中,若碳元素的质量分数为60%,那么可以推断氢元素的质量分数约为
| A.5% | B.8.7% | C.17.4% | D.无法计算 |
下列依据热化学方程式得出的结论正确的是
A.已知2SO2(g)+O2(g)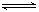 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ |
| D.已知2C(s)+2O2(g)===2CO2(g) ΔH1,2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1<ΔH2 |
下列有关石油和煤的利用叙述不正确的是
A.煤的干馏就是将煤隔绝空气在高温使之分解,得到焦炭.煤焦油等物质的过程
B.煤的液化就是将煤转化成甲醇.乙醇等其液态物质的过程
C.煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程
D .通过催化裂化或裂解,可以获得碳原子数较少的轻质油
.通过催化裂化或裂解,可以获得碳原子数较少的轻质油
下列对化学知识的应用不正确的是
| A.“海水提溴”可用氯气置换溴离子使之成为单质溴 |
| B.糖尿病人病情可用氢氧化铜悬浊液检验 |
| C.沾有油脂的器皿可用热氢氧化钠溶液洗 |
| D.淀粉遇碘变蓝,因此可用碘化钾溶液检验淀粉的存在 |
CH2 = CH—CH2OH的性质可能有
①加成反应②氧化反应③酯化反应④中和反应
| A.只有①③ | B.只有①②③ | C.只有①③④ | D.只有①② |