温度为t℃,压强为1.01×106Pa的条件下,某密闭容器内,下列反应达到化学平衡:A(g) + B(g)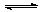 3C,测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×107Pa,第三次达到平衡时,测得c(A)=0.75mol·L-1;则下列关于C物质状态的推测正确的是
3C,测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×107Pa,第三次达到平衡时,测得c(A)=0.75mol·L-1;则下列关于C物质状态的推测正确的是
A.每次平衡时C均为非气态 B.每次平衡时C均为气态
C.第二次达到平衡时C为非气态 D.第三次达到平衡时C为非气态
已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COOH溶液,下列说法正确的是
| A.CH3COONa溶液中,c(CH3COO-)> c(Na+) >c(OH-) >c(H+) |
| B.在相同条件下,两溶液的pH大小为:CH3COONa<NaF |
| C.两溶液相比较,CH3COONa溶液中的离子总数多 |
| D.CH3COONa溶液中,c(H+)+c(CH3COOH)=c(OH-) |
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
| A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B.NaHCO3溶液中:c(H+)+c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| C.中和体积与物质的量浓度都相同的HCl溶液和CH3COOH溶液消耗NaOH物质的量相同 |
| D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同 |
可逆反应mA(固)+nB(气) eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分
eC(气)+fD(气),反应过程中保持其他条件不变,C的体积分
数[j(C)]在温度(T)和压强(P)的条件下随时间(t)变化如下图所示,下列叙述正确的是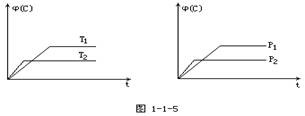
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.达到平衡后,若温度升高,化学平衡向逆反应方向移动
C.化学方程式中n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越
来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为xMg+Mo3S4 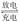 MgxMo3S4;在镁原电池放电时,下列说法错误的是
MgxMo3S4;在镁原电池放电时,下列说法错误的是
| A.Mg2+向正极迁移 |
| B.正极反应为:Mo3S4+2xe-=Mo3S42x- |
| C.Mo3S4发生氧化反应 |
| D.负极反应为:xMg-2xe-=xMg2+ |
在一密闭容器中,反应m A(g)+n B(g) 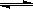 3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是
3 C(g)达到平衡时,测得c(A)=0.5 mol/L。在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)=0.20mol/L。下列判断中正确的是
A.A的质量分数减小 B.化学计量数:m+n >3
C.平衡向右移动 D.物质C的体积分数减小