下列溶液中粒子的物质的量浓度关系正确的是
| A.0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| B.20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L盐酸混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
| C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
下列有关化学用语表示正确的是
| A.二氧化碳结构式:O-C -O |
B.S2-的结构示意图: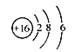 |
C.中子数为146、质子数为92的铀(U)原子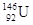 |
D.NH5的电子式为: |
下列说法正确的是
| A.CO2的水溶液能导电,所以CO2是电解质 |
| B.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 |
| C.液溴不导电,所以溴是非电解质 |
| D.BaSO4难溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质 |
向一定量的Cu、Fe2O3的混合物中加人600mL 2mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,再加入过量1 mol/L NaOH溶液,将沉淀过滤、洗涤、干燥,称得质量比原混合物增重17.6g,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量是
| A.4.8 g | B.8.8 g | C.9.6g | D.14.4g |
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO32-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,下列说法正确的是
| A.a点反应的还原剂是NaHSO3,被氧化的元素是碘元素 |
| B.b点反应的离子方程式是:3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O |
| C.c点到d点的反应中共转移0.6mol电子 |
| D.往200mL 1 mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式是:5HSO3-+ 2IO3- =I2+5SO42-+3H++H2O |
工业上正在研究利用CO2来生产甲醇燃料,该方法的化学方程式为CO2(g)+3H2(g) CH3OH(g)+H2O(g)∆H=-49.0kJ/mol,一定温度下,在三个容积均为3.0L的恒容密闭容器中发生该反应:
CH3OH(g)+H2O(g)∆H=-49.0kJ/mol,一定温度下,在三个容积均为3.0L的恒容密闭容器中发生该反应:
| 容器 |
起始物质的量/mol |
平衡物质的量/mol |
|||
| 编号 |
温度/℃ |
CO2(g) |
H2(g) |
CH3OH(g) |
H2O(g) |
| Ⅰ |
T1 |
3 |
4 |
0.5 |
0.5 |
| Ⅱ |
T1 |
1.5 |
2 |
||
| Ⅲ |
T2 |
3 |
4 |
0.8 |
0.8 |
下列有关说法不正确的是
A.若经过2min容器I中反应达平衡,则2min内平均速率V(H2)="0.25" mol/(L·min)
B.达到平衡时,容器I中CO2转化率的比容器Ⅱ的大
C.达到平衡时,容器Ⅲ中反应放出的热量比容器Ⅱ的2倍少
D.若容器Ⅰ、Ⅱ、Ⅲ中对应条件下的平衡常数分别为K1、K2、K3,则K1=K2<K3