氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域有重要用途.
I.工业上有多种方法来制备氮化硅,常见的方法有:
方法一 直接氮化法:在1300℃-1400℃时,高纯粉状硅与纯氮气化合,其反应方程式为 .
方法二 化学气相沉积法:在高温条件下利 用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是 .
用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是 .
方法三 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体(填分子式) ;然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为 .
II.工业上制取高纯硅和四氯化硅的生产流程如下:
已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色.
(1)写出焦炭与原料B中的主要成分反应的化学方程式: .
(2)上述生产 流程中电解A的水溶液的化学方程式: .
流程中电解A的水溶液的化学方程式: .
烷基取代苯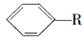 可以被高锰酸钾酸性溶液氧化生成
可以被高锰酸钾酸性溶液氧化生成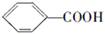 ,但若烷基R中直接与苯环连接的碳原子没有C—H键,则不容易被氧化得到
,但若烷基R中直接与苯环连接的碳原子没有C—H键,则不容易被氧化得到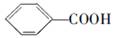 。现有分子式是C11H16的烷基取代苯,已知它可以被氧化成为
。现有分子式是C11H16的烷基取代苯,已知它可以被氧化成为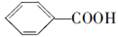 的异构体共有7种。其中3种是
的异构体共有7种。其中3种是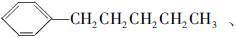
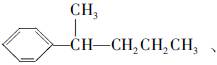
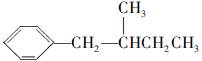
,请写出其他4种的结构简式:_____________,____________,__________,____________。
碳、氢、氧3种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子个数为氧的5倍。
(1)A的分子式是______________。
(2)A有2个不同的含氧官能团,其名称是___________。
(3)一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团。
①A的结构简式是___________。
②A不能发生的反应是(填写序号字母)___________。
a.取代反应 b.消去反应
c.酯化反应 d.还原反应
(4)写出两个与A具有相同官能团并带有支链的同分异构体的结构简式___________、___________。
(5)A还有另一类酯类同分异构体,该异构体在酸性条件下水解,生成两种相对分子质量相同的化合物,其中一种的分子中有2个甲基,此反应的化学方程式是__________________。
(6)已知环氧氯丙烷可与乙二醇发生如下聚合反应:
B也能与环氧氯丙烷发生类似反应生成高聚物,该高聚物的结构简式是______________。
如图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极方程式:
A____________________________________________,
B____________________________________________,
C____________________________________________,
D____________________________________________。
(2)在A、B、C、D各电极上析出生成物的物质的量之比为______________________。
在烷烃分子的基团:—CH3、—CH2—、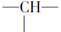 、
、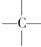 中的碳原子分别称为伯、仲、叔、季碳原子;数目分别用n1、n2、n3、n4表示。如
中的碳原子分别称为伯、仲、叔、季碳原子;数目分别用n1、n2、n3、n4表示。如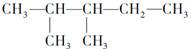 分子中n1=4、n2=1、n3=2、n4=0。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
分子中n1=4、n2=1、n3=2、n4=0。试根据不同烷烃的组成和结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)若烷烃分子中氢原子数为A,A与n1、n2、n3、n4的关系是:
A=_______________,或A=____________。
(2)若分子中n2=n3=n4=1,则该分子的结构简式可能是____________。
(3)四种碳原子数之间的关系是:n1=____________。
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:

(1)正四面体烷的分子式为,其二氯取代产物有种。
(2)关于乙烯基乙炔分子的说法错误的是。
a.能使
酸性溶液褪色
b.1
乙烯基乙炔能与3
发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):、。