乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:

(1)正四面体烷的分子式为,其二氯取代产物有种。
(2)关于乙烯基乙炔分子的说法错误的是。
a.能使酸性溶液褪色
b.1乙烯基乙炔能与3发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:。
(4)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):、。
已知A经如右图所示的过程转化为D,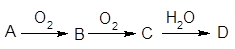
请回答下列问题:
(1)若A为非金属单质,且常温下为淡黄色固体,B为刺激性气味的无色气体,能使品红溶液褪色,D为强酸。
①D的化学式是。
②在工业生产中B气体的大量排放被雨水吸收后形成了而污染了环境。某工厂净化残余的B气体装置如图,则除去B气体的总反应方程式是。
(2)若A是能使酚酞试液变红的气体。D是一种强酸。写出A→B的化学方程式;工业生产上,以34吨A为原料,最多可以生产63%的D酸吨。
下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语回答下列问题:
| 族周期 |
IA |
0 |
||||||
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
② |
③ |
④ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
(1)画出表中形成化合物种类最多元素的原子结构示意图;写出它与原子半径最小的原子形成10电子且为正四面体结构的化合物的电子式_________,用电子式表示⑤和⑧形成化合物的过程________________________________________。
(2)④⑤⑧形成的简单离子半径由大到小的顺序为_______________(填离子符号);③⑦⑨的最高价氧化物对应水化物的酸性由强到弱的顺序为____(填化学式)。
(3)⑤和⑨形成化合物的晶体类型为__________。
(4)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是___________(填化学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式__________。
(5)X、Y由①②④中的两种或三种元素组成。X的溶液能与小苏打反应产生Y,若X是其所属系列中最简单的分子,且相对分子质量为46,则X的名称为,写出X溶液与小苏打反应的化学方程式为_______________。
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标况),实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL) |
50 |
120 |
232 |
290 |
310 |
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5 min)反应速率最大min,原因是;
(2)哪一段时段的反应速率最小min,原因是;
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:A.蒸馏水;BNa2SO4溶液;C.NaNO3溶液;D.CuSO4溶液;E.Na2CO3溶液,你认为可行的
是(填写字母代号)。
(共11分)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法l:还原沉淀法
该法的工艺流程为:
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显色。
(2)能说明第①步反应达平衡状态的是。
A.Cr2O2- 7和CrO2- 7的浓度相同 B.2v(Cr2O2- 7)=v(CrO2- 4) C.溶液的颜色不变
(3)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡: Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)•c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(4)用Fe做电极的原因为。
(5)在阴极附近溶液pH升高的原因是(用电极反应式解释) 。溶液中同时生成的沉淀还有。
为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)=2CO2(g)△H=-566kJ·moL-1
2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ·moL-1
H2O (g)=H2O(l)△H=-44.0KJ·moL-1
(1)氢气的标准燃烧热△H=kJ·moL-1
(2)写出CO和H2O(g)作用生成CO2和H2的热化学方程式
(3)往 1L体积不变的容器中加入1.00mol CO和1.00mol H2O(g),在t℃时反应并达到平衡,若该反应的化学平衡常数K=1,则t℃时CO的转化率为;反应达到平衡后,升高温度,此时平衡常数将(填“变大”、“不变”或“变小”),平衡将向(填“正”或“逆”)方向移动。
(4)在CO和H2O反应转化为绿色能源H2中,为了提高CO的转化率,可采取的措施是。
| A.增大的CO浓度 | B.增大的H2O(g)浓度 | C.使用催化剂 | D.降低温度 |