T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图l所示;若保持其他条件不变,温度分别为T.和T2时,Y的体积百分含量 与时间关系如图2所示。则下列结论错误的是 ( )
与时间关系如图2所示。则下列结论错误的是 ( )
| A.容器中发生的反应可表示为:3X(g)+Y(g)→2Z(g) |
| B.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| C.反应进行的前4 min内,用X表示的反应速率v(X)=0.075mol·(L·min)-1 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
有9.7gCu和Zn的合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2.24L。将溶液稀释为1L,测得溶液的pH=1,此时溶液中NO-3的浓度为
| A.0.3mol/L | B.0.4mol/L | C.0.5mol/L | D.0.6mol/L |
某温度时,用惰性电极电解硝酸钠的不饱和溶液。若两极板收集到气体总体积为22.4aL时,剩余溶液恢复至原温度,析出溶质mg;若两极收集到气体总体积为33.6 aL时,剩余溶液恢复至原温度,析出溶质ng。则硝酸钠在该温度时的溶解度是(气
aL时,剩余溶液恢复至原温度,析出溶质ng。则硝酸钠在该温度时的溶解度是(气 体体积均已折合为标准状况下的体积)
体体积均已折合为标准状况下的体积)
A.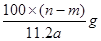 |
B. |
C.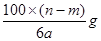 |
D.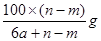 |
下列说法不正确的是
| A.金属元素的最外层电子数不一定小于4 |
| B.1A族元素形成的单质的熔点随原子序数的递增而降低 |
| C.同主族第三、第四周期的元素原子序数之差不一定等于18 |
| D.单质磷的化学性质比氮气活泼,容易与非金属等物质反应 |
对于反应O3+I-+H+—I2+O2+H2O(未配平),下列说法正确的是
| A.O2和H2O是还原产物 |
| B.该反应能说明O2氧化性大于I2 |
| C.氧化产物与还原产物的物质的量之比是1:1 |
| D.配平后的化学方程式为:2O3+2I-+4H+= I2+2O2+2H2O |
已知热化学方程式C2H2(g)+5/2O2(g)=2CO2(g)+H2O(g);△H=-1256kJ/mol,下列说法正确的是
| A.乙炔的燃烧热为1256kJ/mol |
| B.若转移10mol电子,则消耗2.5molO2 |
| C.若生成2mol液态水,则△H=-2512kJ/mol |
| D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ |