水的电离平衡曲线如图所示。下列说法中,正确的是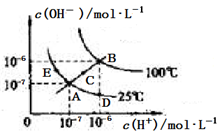
A.图中A、D、E三点处KW间的关系:E处>A处>D处
B.温度不变时,往水中通入适量HCl气体,可以使溶液中的离子浓度从A点变化到D点
C.温度不变时,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到C点
D.在B点处,0.5mol·L-1的H2SO4溶液与1mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7
打开右图所示装置中的止水夹,一段时间后,可能观察到的现象是 ( )
| A.烧杯中有气泡产生 | B.试管内有黄绿色气体产生 |
| C.铁丝网的表面产生锈迹 | D.烧杯内溶液变红色 |
有关热化学方程式书写与对应表述均正确的是 ( )
| A.稀醋酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) △H =" -57.3" kJ·mol-1 |
| B.在101KPa下氢气的标准燃烧热△H =-285.5 kJ·mol-1, 则水分解的热化学方程式: 2H2O(l)=2H2(g)+O2(g) △H =" +285.5" kJ·mol-1 |
| C.密闭容器中,9.6 g硫粉与11. 2 g铁粉混合加热生成硫化亚铁17 .6 g时,放出19.12 kJ热量。 则Fe(s)+S(s)="FeS(s)" △H=" -" 95.6 kJ·mol-1 |
| D.已知2C(s)+O2(g)="2CO(g)" △H=-221 kJ·mol-1,则可知C的标准燃烧热为110.5 kJ·mol-1 |
下列说法正确的是( )
| A.据能量守恒定律,反应物的总能量一定等于生成物的总能量 |
| B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
在密闭容器中发生可逆反应4NH3+5O2 4NO+6H2O(g),以下是不同情况下的反应速率
4NO+6H2O(g),以下是不同情况下的反应速率 ,其中最快的是( )
,其中最快的是( )
| A.v(O2)="0.01" mol·L-1·s-1 | B.v(NH3)="0.02" mol·L-1·s-1 |
| C.v(H2O)="0.04" mol·L-1·s-1 | D.v(NO)="0.03" mol·L-1·s-1 |
下列说法不正确的是
| A.焓变是一个反应能否自发进行相关的因素,多数放热反应能自发进行 |
| B.自发进行的反应一定能迅速进行 |
| C.在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| D.一个反应能否自发进行,与焓变和熵变的共同影响有关 |