下列反应的离子方程式书写正确的是
| A.漂白粉溶液中通入过量二氧化碳气体:2ClO﹣ + CO2 + H2O="2HCIO" + CO32- |
| B.用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O |
| C.NH4HCO3溶液中加入过量NaOH溶液:NH4++OH﹣=NH3·H2O |
| D.在NaHCO3溶液中加入少量石灰水:2HCO3﹣+2OH﹣+Ca2+=CaCO3↓+ CO32-+2H2O |
下列元素不属于主族元素的是()
| A.P | B.Ca | C.Fe | D.Cl |
下图表示反应X(g)  4Y(g) +Z(g);在某温度时X的浓度随时间变化的曲线。下列有关该反应的描述正确的是()
4Y(g) +Z(g);在某温度时X的浓度随时间变化的曲线。下列有关该反应的描述正确的是()
| A.第6min后,反应就停止了 |
| B.X的平衡转化率为85% |
| C.反应只进行了6min |
| D.在1min内X的平均反应速率为0.7 mol·L-1·min-1 |
下列各表分别是元素周期表的一部分,表中的数字表示元素的原子序数,各表中数字所表示的元素在周期表中的位置与周期表的结构相符的是() v
v
判断在下列装置中电流表能发生偏转的是()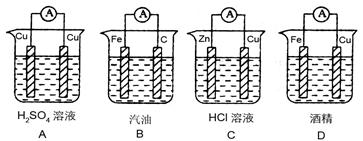
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)  2C(g),若经2s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,正确的是()
2C(g),若经2s后测得C的浓度为0.6 mol·L-1,现有下列几种说法,正确的是()
①用物质A表示该反应的平均反应速率为0.3 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
| A.①③ | B.①④ | C.②③ | D.③④ |