已知:HCN的结构为H—C≡N;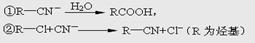
玉米芯、甘蔗渣等废物水解发酵后可制得糠醛 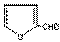 它是重要的化工原料,它在一定条件下可发生以下变化:
它是重要的化工原料,它在一定条件下可发生以下变化:
⑴写出反应类型:② ,④ 。
⑵写出反应③的化学方程式: ;
写出能证明糠醛中含有醛基的一个化学反应 方程式:
方程式:
。
⑶若E为环状化合物,则其结构简式 。
⑷若E为高聚物,则其结构简式 。
(5)玉米芯、甘蔗渣水解的产物 之一J,在酵母菌的作用下产生了一种温室气体Q和另一种有机物W。①写出Q的电子式: ;②写出实验室用W制取一种能使溴的四氯化碳溶液褪色的气体P的化学方程式: ;③将光亮的铜丝在酒精灯的外焰灼烧片刻后,再缓缓移入内焰,观察到铜丝又变得光洁无暇。请用最简洁的语言释之: 。
之一J,在酵母菌的作用下产生了一种温室气体Q和另一种有机物W。①写出Q的电子式: ;②写出实验室用W制取一种能使溴的四氯化碳溶液褪色的气体P的化学方程式: ;③将光亮的铜丝在酒精灯的外焰灼烧片刻后,再缓缓移入内焰,观察到铜丝又变得光洁无暇。请用最简洁的语言释之: 。
工业上制取CuSO4,不是直接用浓H2SO4与铜加热的条件下反应,而是将铜丝浸入稀H2SO4中并不断的由容器的下部吹入细小的空气泡。试分析这种制取方法的优点是______。
在25℃时若10体积某强酸溶液与1体积的某强碱溶液混合后溶液是碱性,则混合前,该强酸的溶液的pHX与该强碱溶液的pHY之间应满足的关系是______。
对复杂的有机物的结构可用“键线式”简化表示,如苯丙烯酸丙烯酯:
可简化为: ,杀虫剂“阿乐丹”的结构表示为:
,杀虫剂“阿乐丹”的结构表示为:
(1)它的化学式为______。
(2)若它在稀酸作用下能生成两种有机物,这两种有机物可能有的共同性质是
| A.遇FeCl3溶液均显紫色 |
| B.均与NaOH溶液反应 |
| C.在一定条件下均与H2反应 |
| D.均能与溴水发生加成反应 |
地球外层空间存着微量的臭氧和氧原子。该臭氧层能吸附太阳的有害的紫外线辐射。可是人为的</PGN0075B.TXT/PGN>大气污染物破坏臭氧层,如超音速飞机排放物含NO和NO2,与O3与O可发生:O3+NO====NO2+O2;O+NO2====NO+O2的反复循环反应,其总反应方程式______。由此可见氮的氧化物在破坏臭氧层过程中起了______作用。
A、B两种物质都是由氢、氮、氧、钠四种元素中的任意三种元素组成,它们的水溶液分别呈酸性或碱性。在相同温度下A溶液的pH大于相同浓度的B溶液的pH(溶液浓度不大于10-5mol/L)。请找出A和B可能有的两种组合,并且要求当这两种组合中的B溶液的pH相等时,第一种组合的B溶液中水的电离度小于第二种组合的B溶液中水的电离度。
(1)写出可能有的两种组合中A和B的化学式:第一种组合,A是______;B是______。第二种组合,A是______,B是______。
(2)说明pH相等时,第一种组合的B溶液中水的电离度比第二种组合的B溶液中水的电离度小的原因:______。
(3)在上述的第一种组合中,若A,B的物质的量浓度相同且温度相同,设A溶液中水的电离度是α1,B溶液中水的电离度是α2,那么α1和α2的关系式是______。