A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体。E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶于水成为无色溶液,G溶于水得棕黄色溶液。这九种物质间反应的转化关系如下图所示
(1)写出四种单质的化学式
A_________ B________ C_________ D________
(2)写出E+F→H+I的离子方程式 ;
(3)写出G+I→H+D+E的化学反应方程式 。
有一种透明溶液,做如下实验:
①取少量该溶液滴入用盐酸酸化的BaCl2溶液中,有白色沉淀生成,无其他现象。
②另取少量该溶液加入Na2O2,有无色无味的气体放出,且有白色沉淀生成,加入Na2O2的
量与沉淀量关系如下图所示。试回答: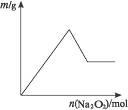
(1)在Cu2+、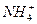 、Al3+、Mg2+、Na+、
、Al3+、Mg2+、Na+、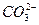 、
、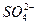 等离子中一定存在________________,一定不存在____________________________________________________________________。
等离子中一定存在________________,一定不存在____________________________________________________________________。
(2)判断该物质溶解的溶质是_____________________________________________________。
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定的条件下可实现下图所示的物质之间的变化: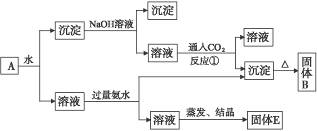
据此判断:
(1)固体B所含物质的化学式为________________________________________________。
(2)固体E所含物质的化学式为________________________________________________。
(3)反应①的离子方程式为_____________________________________________________。
在一定温度下,把2 mol SO2和1 mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O2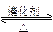 2SO3。当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c、分别代表初始加入的SO2、O2和SO3的物质的量(摩)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同。请填写下列空白:
2SO3。当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c、分别代表初始加入的SO2、O2和SO3的物质的量(摩)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同。请填写下列空白:
(1)若a=0,b=0,c=_____________。
(2)若a=0.5,则b=_____________和c=____________。
(3)a、b、c取值必须满足的一般条件是(用两个方程式表示,其中一个只含a和c,另一个只含b和c):_____________,______________。
恒压(1.01×105 Pa)下,将2.0 mol SO2与a mol O2的混合气体通入一个容积可变的密闭容器中,发生如下反应:
2SO2(g)+O2(g) 2SO3(g);ΔH<0
2SO3(g);ΔH<0
(1)T1℃下反应达平衡时,测得容器内n(SO3)="1.3" mol,n(O2)="3.0" mol,则a=_______________;平衡时SO2的转化率为__________________。
(2)T2℃下反应达平衡时,混合气体的物质的量共为4.8 mol。T1与T2的关系是___________(选填序号)。
①T1>T2②T1<T2③T1=T2
一定条件下,在容积为2 L的密闭容器中将2 mol 气体N和3 mol气体M混合,发生如下反应:
2N(g)+3M(g) xQ(g)+3R(g),当反应达到平衡时,生成2.4 mol气体R,并测得Q的浓度为0.4 mol·L-1。x的值为_________,N的转化率为_________。
xQ(g)+3R(g),当反应达到平衡时,生成2.4 mol气体R,并测得Q的浓度为0.4 mol·L-1。x的值为_________,N的转化率为_________。