科研、生产中常涉及钠、硫及其化合物。
(1)实验室可用无水乙醇处理少量残留的金属钠,化学反应方程式为。要清洗附着在试管壁上的硫,可用的试剂是。
(2)右图为钠硫高能电池的结构示意图,该电池的工作温度为320左右,电池反应为,正极的电极反应式为。(由和制得)的两个作用是。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的倍。

(3)溶液中离子浓度由大到小的顺序为,向该溶液中加入少量固体,溶液(填"增大""减小"或"不变"),溶液长期放置有硫析出,原因为(用离子方程式表示)。
某化学反应 3 A  2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:
2 B + D在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验 1 ,反应在10 min ~20 min 内平均速率为_______ mol /(L·min)
(2)在实验 2 ,A 的初始浓度 C2 _______ mol / L ,反应经 20 min 就达到平衡,可推测实验 2 中还隐含的条件是____________________________
(3)设实验 3 的反应速率为 v3,实验 1 的反应速率为 v1,则 v3 ____v1 (填 <、>或=),
且C3 ______ 2.0 mol / L (填 <、>或=)
(4)比较实验 4 和实验 1,可推测正反应是______反应(填吸热或放热)。理由是__________
(5)该反应化学平衡常数表达式为。
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池.
①当电解质溶液为稀硫酸时:
Cu电极是_____(填“正”或“负”)极,其电极反应为____,该反应是____(填“氧化”或“还原”)反应;
②当电解质溶液为浓硝酸时:
Cu电极是_____极,其电极反应为__________,该反应是_____反应.
(2)电解是将能转化为能。请写出电解硫酸铜溶液的总化学方程式____________
(3)燃烧氢气时耗氧量小,发热量大.已知4克H2燃烧生成液态水时放热为571.6kJ,试写出表示H2燃烧热的热化学方程式为:.
(4)下图是一碳酸盐燃料电池(MCFC),以水煤气(CO、H2)为燃料,一定比例Li2CO3和Na2CO3低熔混合物为电解质。写出B极发生的电极反应式。
(1)AgNO3的水溶液呈(填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”、“抑制”)其水解。
(2)醋酸钠水溶液PH7 ,(填“>”、“=”、“<”)
原因是(用离子方程式表示):____________________________________ 。
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是。
(3)氯化铵溶液中滴加适量氨水,至溶液呈中性,则
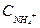 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
结构决定性质,性质体现结构。对结构和性质的研究是学好化学的基础。
(1)下列4种物质熔点沸点由高到低排列为______________(填序号)
①金刚石(C—C) ②晶体硅(Si—Si) ③金刚砂(Si—C)
(2)某晶体的晶胞如图所示,X位于体心,Y位于4个面心,Z位于8个
顶点,该晶体中 X、Y、Z的粒子个数比为______________;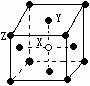
(3)按所示格式填写下表有序号的表格:
| 原子序数 |
原子价层电子排布 |
周期 |
族 |
| 17 |
① |
第三 |
② |
| ③ |
3d54s1 |
④ |
ⅥB |
(4)某元素的激发态原子的电子排布式为1s 2s
2s 2p
2p 3s
3s 3p
3p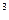 4s
4s ,则该元素基态原子的电子排布式为 ;其最高价氧化物对应的水化物的化学式是。
,则该元素基态原子的电子排布式为 ;其最高价氧化物对应的水化物的化学式是。
(12分)一定温度下,向如图所示带有可移动活塞的密闭容器中充入2 L SO2和1 L O2的混合 气体,发生如
气体,发生如 下反应2 SO2 (g) + O2 (g)
下反应2 SO2 (g) + O2 (g) 
 2 SO3 (g) 。
2 SO3 (g) 。
(1) 若活塞可自由移动,平衡后,活塞停止在“2.1”处该反应中SO2的转化率为。
(2) 若开始时,充入容器的起始物质分别是
①2 L SO2和1 L O2;
②2 L SO3 (g) 和 1 L N2 ;
③1 L SO2、1 L O2和 1 L SO3 (g),
使活塞固定在“3”处,达到平衡后,容器中SO3 (g)占反应混合物的体积分数的大小关系是:(用序号①②③和“<”、“=”、“>”表示)。
(3) 向(1)平衡后的容器中充入0.2 mol 的SO3,活塞移动后再次达到平衡时,测得此过程中从外界共吸收了1.96 kJ 的热量。写出SO2发生氧化反应的热化学方程式:
_______________。