以下有关原子结构及元素周期律的叙述正确的是()
| A. |
以ⅠA族元素铯的两种同位素比多4个质子 |
| B. |
同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C. |
第ⅦA族元素从上到下,其氢化物得稳定性逐渐增强 |
| D. |
同主族元素从上到下,单质的熔点逐渐降低 |
在预防SARS时,医学专家告诉我们对公共场所要进行消毒,毛巾、口罩要经常用开水蒸煮,被褥要放在太阳光下直射,其目的是
| A.使多糖水解 | B.使油脂水解 | C.使氨基酸变性 | D.使蛋白质变性 |
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g)△H=-92.6kJ·mol-1
2XY3(g)△H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 编号 |
起始时各物质物质的量/mol |
||
| X2 |
Y2 |
XY3 |
|
| ① |
1 |
3 |
0 |
| ② |
0.6 |
1.8 |
0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
某元素的原子最外电子层排布是6s26p4,该元素或其化合物不可能具有的性质是
| A.该元素单质可能是导体 |
| B.该元素的最高化合价呈+6价 |
| C.该元素能与氢气反应生成气态氢化物 |
| D.该元素价电子轨道中有2个未成对电子 |
下列物质分类的正确组合是
| 分类 组合 |
纯净物 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
| A |
碱石灰 |
乙二酸 |
纯碱 |
氧化铝 |
二氧化碳 |
| B |
盐酸 |
石炭酸 |
小苏打 |
氧化镁 |
二氧化氮 |
| C |
H2O2 |
硬脂酸 |
苏打 |
过氧化钠 |
二氧化硫 |
| D |
五水硫酸铜 |
油酸 |
碱式碳酸铜 |
氧化钠 |
三氧化硫 |
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH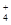 )> c(SO )> c(SO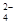 )>c(Fe2+)>c(H+) )>c(Fe2+)>c(H+) |
B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO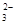 )+c(HCO )+c(HCO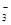 )+c(OH-) )+c(OH-) |
C.0.1 mol·L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO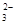 ) ) |
| D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中: |
c (CH3COO-) > c (Na+) > c (H+)> c (OH-)