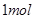 某烷烃可与
某烷烃可与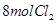 完全取代,则此烷烃的分子式为( )
完全取代,则此烷烃的分子式为( )
| A.CH4 | B.C2H6 | C.C3H8 | D.C4H10 |
下列关于化学键的说法正确的是
| A.构成单质分子的微粒一定含有共价键 |
| B.全部由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性键只存在于双原子单质分子中 |
| D.不同元素组成的多原子分子里的化学键一定都是极性键 |
下表中金属的冶炼原理与方法不匹配的是( )
| 冶炼原理 |
方法 |
|
| A |
2HgO 2Hg + O2 ↑ 2Hg + O2 ↑ |
热分解法 |
| B |
 |
电解法 |
| C |
Cu2S+ O2 2Cu + SO2 2Cu + SO2 |
热分解法 |
| D |
Fe2O3 + 2Al 2 Fe + Al2O3 2 Fe + Al2O3 |
热还原法 |
为实现消除碘缺乏症的目标,常采取向食盐中加入含碘的物质。其中的碘以碘酸钾(KIO3)形式存在。已知在溶液中IO3- 和I- 可发生反应:IO3-+ I-+6H+==3I2+3H2O。根据上述反应,可用试纸和一些生活中常见的物质进行实验,证明食盐中存在IO3-。可供选用的物质有:①自来水;②蓝色石蕊试纸;③碘化钾淀粉试纸;④淀粉;⑤食糖;⑥食醋;⑦白酒。进行上述实验时必须使用的物质是()
| A.③⑥ | B.②④⑥ | C.①③ | D.①②④⑤⑦ |
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片与稀H2SO4的反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的炭与CO2的反应 | D.甲烷在O2中的燃烧反应 |
化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的是()
①用电子式表示HCl的形成过程: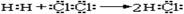
②MgCl2的电子式: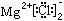
③质量数为133、中子数为78的铯原子: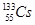
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图: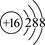
| A.①②③④⑤ | B.④⑤ | C.③④ | D.③⑤ |